دوره 25، شماره 4 - ( زمستان 1403 )
دوره، شماره، فصل و سال، شماره مسلسل |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Gallego-Peñalver F J, Cía-Blasco P, Gómez-Trullén E M. Unilateral Psoas Muscle Atrophy as a Possible Risk Factor for Low Back Pain After Total Hip Arthroplasty: A Case Report. jrehab 2025; 25 (4) :890-905
URL: http://rehabilitationj.uswr.ac.ir/article-1-3463-fa.html
URL: http://rehabilitationj.uswr.ac.ir/article-1-3463-fa.html
گالگو پنالور فرانسیسکو خوزه، سیا بلاسکو پدرو، گومز ترویین اوا ماریا. آتروفی یکطرفه عضله پسوآس بهعنوان ریسک فاکتور بروز کمردرد پس از تعویض کامل مفصل ران: گزارش موردی. مجله توانبخشی. 1403; 25 (4) :890-905
URL: http://rehabilitationj.uswr.ac.ir/article-1-3463-fa.html
1- گروه طب فیزیکی و پرستاری، دانشکده ساراگوسا، گروه تحقیقاتی IIS، آیهلثی (iHealthy) آراگون، دانشگاه ساراگوسا، ساراگوسا، اسپانیا. ، franciscojosegp@gmail.com
2- بخش توانبخشی، بیمارستان اوبیسپو پولانکو، بیمارستان، تروئل، اسپانیا.
3- واحد درد، کلینیک دانشگاه لوزانو بلسا، ساراگوسا، اسپانیا.
2- بخش توانبخشی، بیمارستان اوبیسپو پولانکو، بیمارستان، تروئل، اسپانیا.
3- واحد درد، کلینیک دانشگاه لوزانو بلسا، ساراگوسا، اسپانیا.
متن کامل [PDF 2231 kb]
(652 دریافت)
| چکیده (HTML) (5445 مشاهده)
متن کامل: (1002 مشاهده)
مقدمه
درد ناحیه کمری بسیار شایع است و یکی از علل اصلی ناتوانی کاری در جوانان به شمار میرود. برآورد میشود که دوسوم بزرگسالان در مقطعی از زندگی خود درد ناحیه تحتانی کمر (LBP) را تجربه میکنند و ۱۰ درصد از آنها به درد ناحیه تحتانی کمر مزمن مبتلا خواهند شد [۱]. یکی از شایعترین علل درد ناحیه تحتانی کمر، انحطاط دیسک بین مهرهای است. عوامل متعددی باعث انحطاط دیسک بین مهرهای میشوند و در بیشتر موارد فعالیتهای شغلی و سبک زندگی، بهویژه عواملی مانند چاقی و سیگار در این زمینه نقش دارند [۲]. روند پیری ازنظر فیزیولوژیکی به انحطاط دیسک بین مهرهای کمک میکند. تخمین زده میشود که در سن ۷۰ سالگی، محتوای آب هسته پالپوزوس تا ۷۰ درصد کاهش مییابد [۳]. سایر عواملی که روند انحطاط را تسریع میکنند عبارتاند از بیماریهای عفونی، فرآیندهای التهابی، تروما یا تغییرات بیومکانیکی [۲، ۴]. علاوهبر عوامل ذکر شده ، تغییرات در عملکرد عضلانی و عوامل بیومکانیکی نقش مهمی در ایجاد و تشدید درد ناحیه تحتانی کمر دارند [۵]. کاستیهای موجود در قدرت و هماهنگی عضلات ممکن است به الگوهای بارگذاری غیرطبیعی بر روی ستون فقرات کمک کنند که این امر فرآیندهای انحطاط را تشدید کرده و خطر ابتلا به درد ناحیه تحتانی کمر را افزایش میدهد [۶].
درک تعامل پیچیده موجود بین عوامل بیومکانیکی و عملکرد عضلات در درد ناحیه تحتانی کمر نقش مهمی در شناخت شرایط مرتبط، مانند عوارض احتمالی تعویض مفصل کامل ران دارد. مطالعات اخیر نشان میدهند که بین تعویض کامل مفصل ران (THA) و آتروفی یکطرفه عضله پسوآس (PM) در سمت ایمپلنت ارتباطی وجود دارد که نشاندهنده این است که این آتروفی احتمالاً عارضه دیرهنگام جراحی باشد [۷]. محل عضله پسوآس آن را به یک تثبیتکننده مهم ستون فقرات تبدیل میکند که بر وضعیت استاتیک و پویایی ستون فقرات کمری تأثیر میگذارد [۸، ۹]. آتروفی عضله پسوآس بهطور قابلتوجهی بر بیومکانیک ستون فقرات کمری تأثیر میگذارد و ممکن است در ایجاد بیماریهای انحطاط دیسک نقش داشته باشد.
در این زمینه، مقاله حاضر مورد بالینی مرد ۵۳ سالهای را که قبلاً تحت درمان تعویض کامل مفصل ران راست قرار گرفته بود، ارائه میکند. 8 سال پس از جراحی، بیمار به وضعیت مزمن Lumbo-sciatalgia دچار شد که پای چپ را تحت تأثیر قرار میداد و همچنین ضعف در خم شدن ران راست را منجر میشد. تحلیلهای بالینی و رادیولوژیک وجود فتق دیسک L5–S1 بیرون برآمده شده و آتروفی یکطرفه عضله پسوآس در همان سمت تعویض مفصل را نشان داد.
درحالیکه بیمار با رویکرد دارویی و توانبخشی محافظهکارانه بهبود یافت، بهبودی کامل، احتمالاً بهدلیل طولانی شدن دوره بهبودی وضعیت وی حاصل نشد. این بهبودی طولانیمدت میتوانست آسیبهای جبرانناپذیری به ساختارهای آناتومیکی آسیبدیده وارد کند و توانایی بیمار را برای بهبودی کامل محدود کند. این مقاله به بررسی مورد بالینی خواهد پرداخت، ارتباط بین آتروفی عضله پسوآس و تحلیل دیسک لومباری را بررسی کرده و بر اهمیت تشخیص زودهنگام و مدیریت جامع در بیماران مبتلا به آتروفی عضله پسوآس پس از تعویض مفصل کامل لگن ران تأکید خواهد کرد.
گذشته از ارائه مورد منحصربهفرد، این مورد بالینی بهعنوان نقطه شروع یک تلاش تحقیقاتی درحالانجام عمل کرده و ارزش آن را در حوزه پزشکی و عمل بالینی روزمره، بهویژه در توانبخشی، مورد تأکید قرار میدهد.
مورد بالینی
مردی ۵۳ ساله با درد حاد عصب سیاتیک چپ به واحد خدمات اورژانس بیمارستان کلینیک دانشگاه لوزانو بلسا مراجعه کرد. او در ۱۲ ساعت گذشته قبل از رسیدن به بخش اورژانس از این درد رنج میبرد و شدت آن در مقیاس عددی ۹ از ۱۰ ارزیابی شده بود. بیمار هرگونه سابقه درد ناحیه تحتانی کمر یا انتشار درد به پا قبل از مراجعه را رد کرد. این درد مکانیکی به اندام تحتانی چپ منتشر میشد که به مچ پا و انگشت شست پا گسترش مییافت. بیمار در زمان پذیرش علائم تب نداشت و اخیراً ترومایی را تجربه نکرده بود. کشش رادیکولار و آزمایشهای مثبت لازگ و براگارد درد را تشدید کرد. معاینه فیزیکی بیشتر نشان داد که بیمار درد در عضلات چهارگوش کمری و عضلات راستکننده ستون فقرات داشت و درد از پشت پا به سمت پا منتشر میشد.
ضعف حرکتی ۲ از ۵ در سیستم درجهبندی عضلانی کندال در اکستنشین انگشت شست پای چپ و در فلکسیون پلانتار مچ پای چپ مشاهده شد. همچنین ضعف متوسط ۲ از ۵ در فلکسیون ران راست وجود داشت و سایر میوتومهای lumbosacral طبیعی بودند. معاینه حسی نشان داد در درماتوم S1 سمت چپ هیپوستزی و هیپوآلژزی وجود دارد، اما در سایر درماتومها تغییری مشاهده نشد. هیچ اختلال حسی مرتبط با cauda equina مشاهده نشد و نشانهای از اختلال عملکرد اسفنکتر تشخیص داده نشد.
شرح حال و ارزیابی رادیولوژیکی
با بررسی سابقه پزشکی بیمار، متوجه شدیم که او در آوریل ۲۰۱۲ بهدلیل ککسارتروز تکطرفه پیشرفته در طی 2 سال گذشته، عمل تعویض مفصل ران راست را انجام داده است و 4 هفته پس از جراحی، بیمار 6 جلسه فیزیوتراپی را انجام داد. در این جلسات به بیمار آموزش داده شد و ارزیابی شد که چگونه علاوهبر بازآموزی راه رفتن، تمرینات تقویت عضلانی برای لگن (عضلات گلوتئال، ایلیوپسوآس، ادکتورها، چهارسر ران و همسترینگها) را انجام دهد. بیمار از ضعف خفیف در فلکسیون لگن راست و درد در ناحیه کشاله ران راست گزارش داد، اما هیچ دردی در ناحیه کمری وجود نداشت. این علائم بهعنوان عوارض شایع پس از جراحی در نظر گرفته شد. عمل تعویض مفصل ران که از طریق رویکرد جانبی با پروتز SL-Plus+Epfit انجام شد، بهعنوان پاسخ به استئوآرتریت لگن درجه ۳ طبق طبقهبندی کِلگرن–لارنس (تصویر شماره ۱) نشان داده شد.
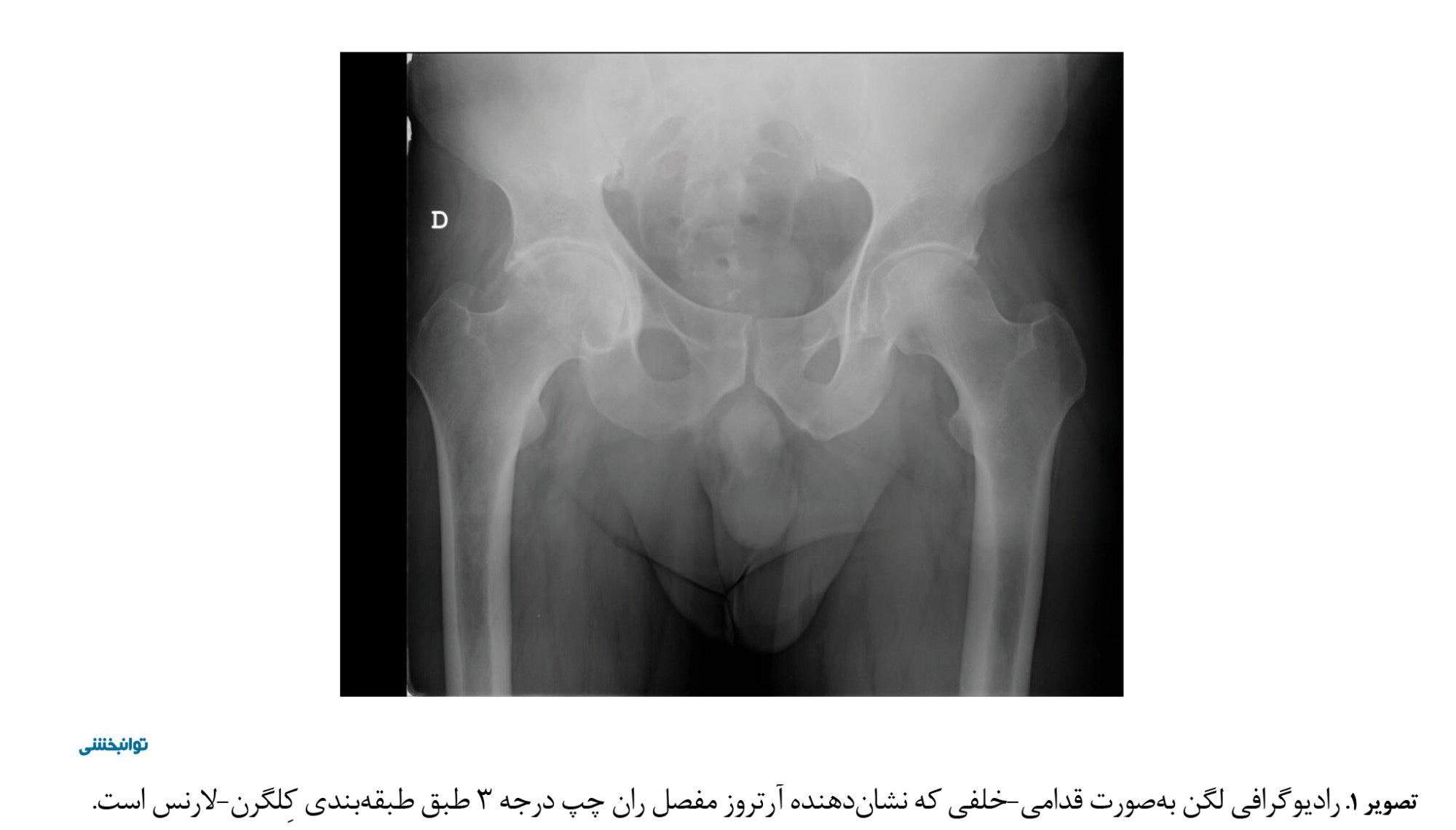
شاخص توده بدنی 29/58 کیلوگرم بر مترمربع بود. اشعه ایکس ناحیه کمری نتایج قابلتوجهی را نشان نداد، اما تصویربرداری تشدید مغناطیسی (MRI) ناحیه کمری وجود فتق دیسک پارامدین چپ در سطح L5–S1 را نشان داد که با قطعهای از دیسک بینمهرهای حجیم که از محل اصلی خود جدا شده بود در extraforaminal همراه بود (تصویر شماره 2).
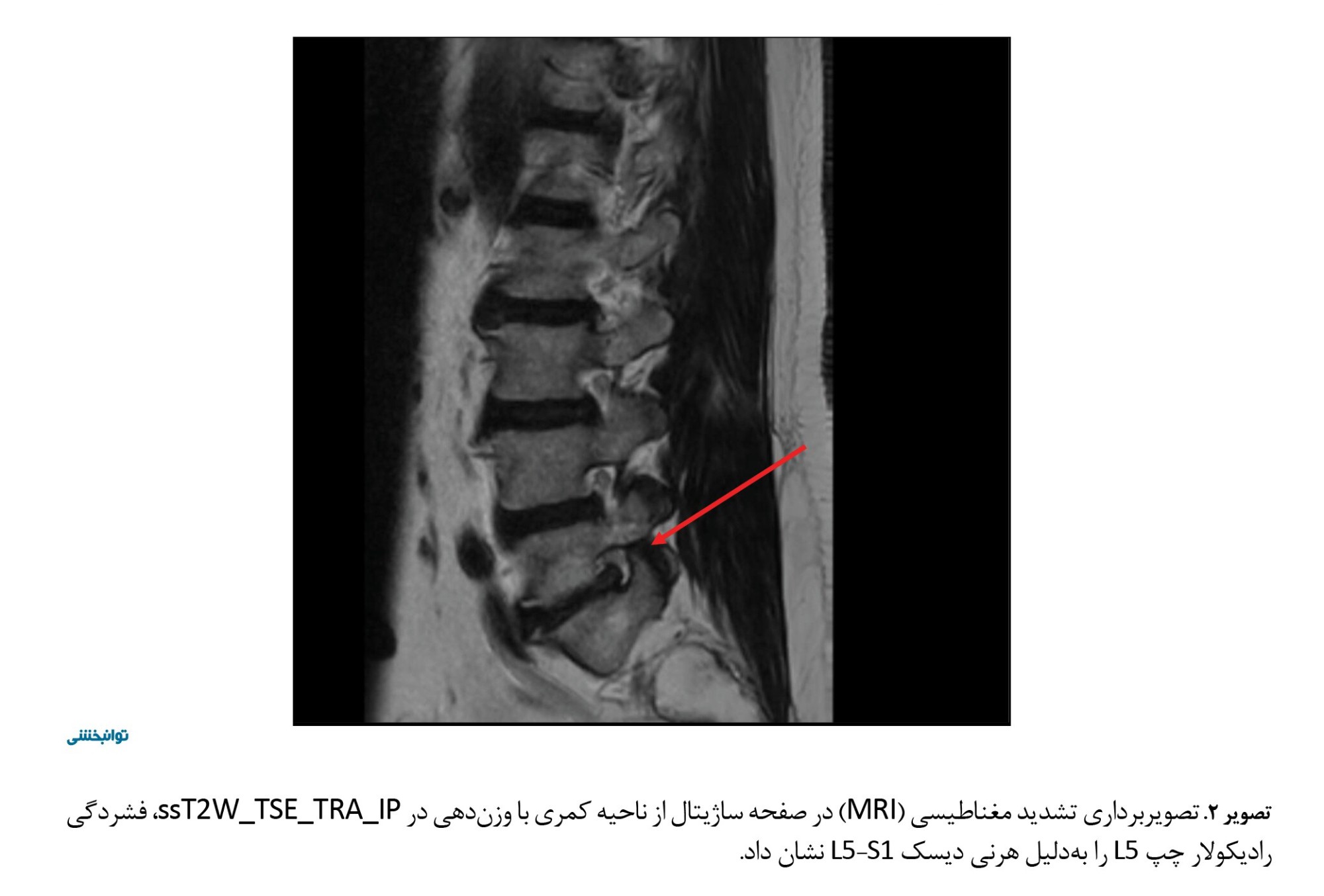
آتروفی قابلتوجهی از عضله پسوآس راست مشخص بود و با نفوذ بافت چربی در همان ناحیه تشدید شده بود. مساحت مقطع عرضی (CSA) عضله پسوآس بهطور دوطرفه توسط یک رادیولوژیست در دیسک بینمهرهای L3–L4 اندازهگیری شد و مساحتی معادل ۶۸۱ میلیمتر مربع در سمت راست بهدست آمد که نمره گوتالیه ۳ نشاندهنده آتروفی شدید عضلانی بود. سمت چپ مساحتی معادل ۱۳۸۸ میلیمتر مربع داشت و نمره گوتالیه صفر بود (تصویر شماره ۳ الف). شاخصهای مساحت مقطع عرضی عضله پسواس/دیسک در سمت راست و چپ بهترتیب 0/49 و 0/99 محاسبه شد. تصویربرداری، تشدید مغناطیسی بخشهایی از عضله پسوآس بدون شکم عضلانی را نشان داد (تصویر شماره ۳ ب). این یافتهها آسیبشناسی را نشان دادند و بیماریهای دیگر عصبی-عضلانی و بیماریهای سیستم عصبی مرکزی را رد کردند.
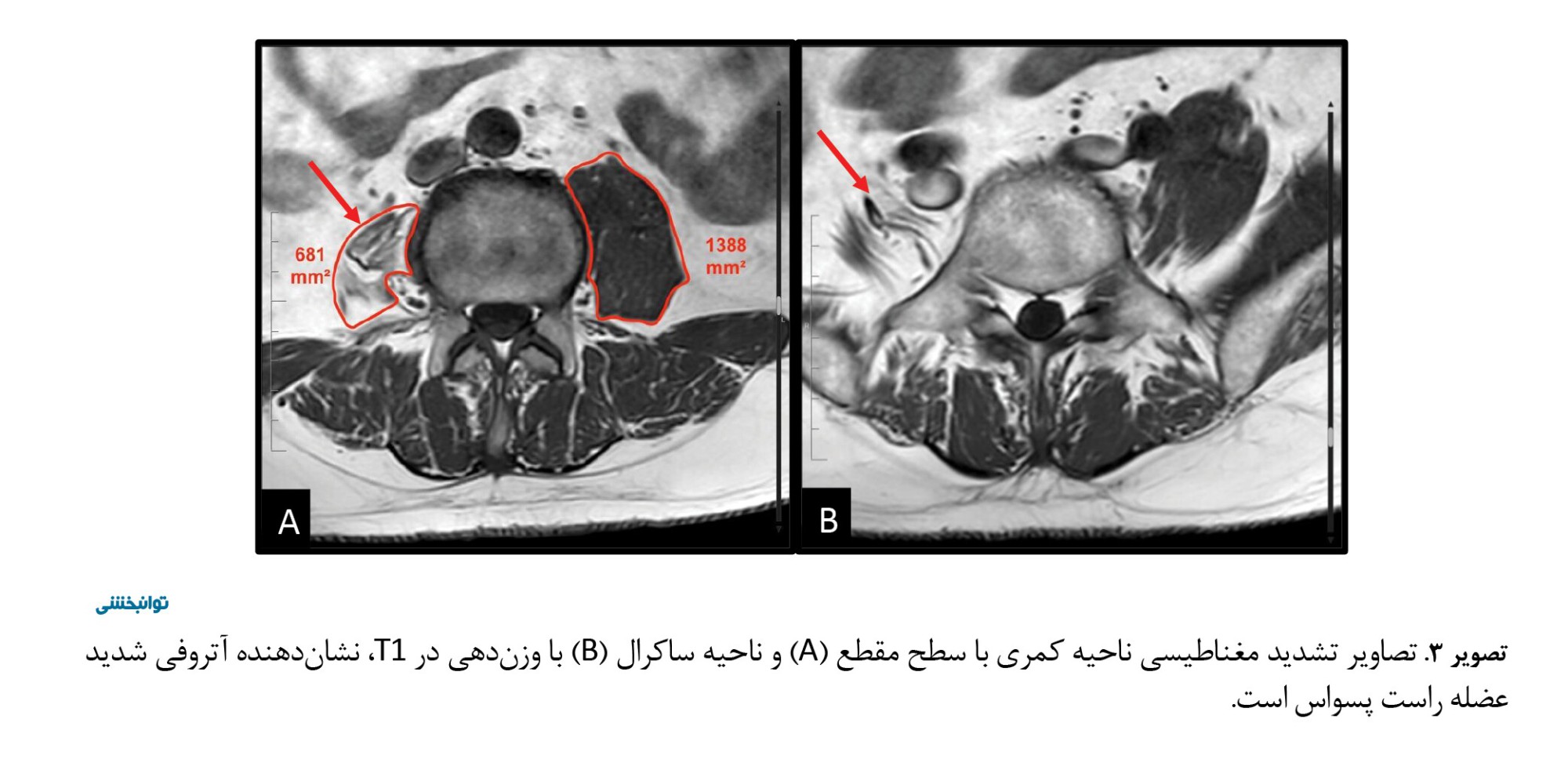
بهبود
بهدلیل شدت درد و تظاهرات بالینی، بیمار در بخش جراحی مغز و اعصاب بستری شد و تحت درمان با داروهای ضددرد مشتق از مواد افیونی (مسکنهای قوی) قرار گرفت. علاوهبراین، تزریق اپیدورال دمی با بیحسکننده موضعی و کورتیکواستروئید انجام شد که به پاسخ مطلوب منجر شد. بیمار پس از 2 روز بستری شدن ترخیص شد و یک برنامه توانبخشی از طریق ۱۵ جلسه فیزیوتراپی با تمریناتی که بر تقویت عضلات خمکننده سمت راست لگن متمرکز بود، آغاز گردید. در این برنامه بهویژه به عضله پسواس، تمرینات تثبیتکننده لومبوپلویک، کششهای عضلات راستکننده کمر، تحریک الکتریکی عصب از راه پوست برای تسکین درد و دینامیک عصبی عصب سیاتیک توجه ویژهای شد. بازآموزی راه رفتن نیز بخشی اساسی از برنامه درمانی بود که به اصلاح الگوهای غیرطبیعی ضددرد و بهبود دینامیک حرکتی کمک کرد. یک الکترومیوگرام که بهصورت سرپایی انجام شد، الگوی مزمن رادیکولار رنج و دنوورهسازی ریشه چپ S1 را نشان داد.
علیرغم تلاشهای مداوم در درمان محافظه کارانه و توانبخشی، تداوم درد و درگیری رادیکولار به مرحله جدیدی از درمان منجر شد. باتوجهبه مدت طولانی علائم که حدود ۲۴ ماه به طول انجامید و عدم پاسخ رضایتبخش به اقدامات غیرجراحی، مداخله جراحی در فوریه ۲۰۲۱ ضروری بود. درنهایت، جراحی از طریق میکرو دیسککتومی و فارامینوتومی چپ L5–S1 انجام شد که بهطور موفقیتآمیزی درد را بهمدت حدود ۱۲ ماه تسکین داد. 1 سال بعد، بیمار دوباره با رادیکولاپاتی چپ L5 بدون نقص حسی یا حرکتی مراجعه کرد. آخرین MRI ناحیه کمری، فتق دیسک میدیوپارامدیکال و پستولترال سمت چپ در سطح L4–L5 را نشان داد. این فتق بالاتر از فتق دیسکی که قبلاً درمانشده بود قرار داشت که همراه با حرکت مختصر caudal که با ریشه چپ L5 تماس قابلتوجه و وسیعی داشت بود (تصویر شماره ۴). باتوجهبه یافتههای درد رادیکولار چپ L5 بدون نقص عصبی در نواحی دورتر از ناحیه آسیبدیده در آخرین معاینه فیزیکی، بیمار تحت نظر بخش مدیریت و درمان درد برای ارزیابی و مدیریت بیشتر قرار گرفت.
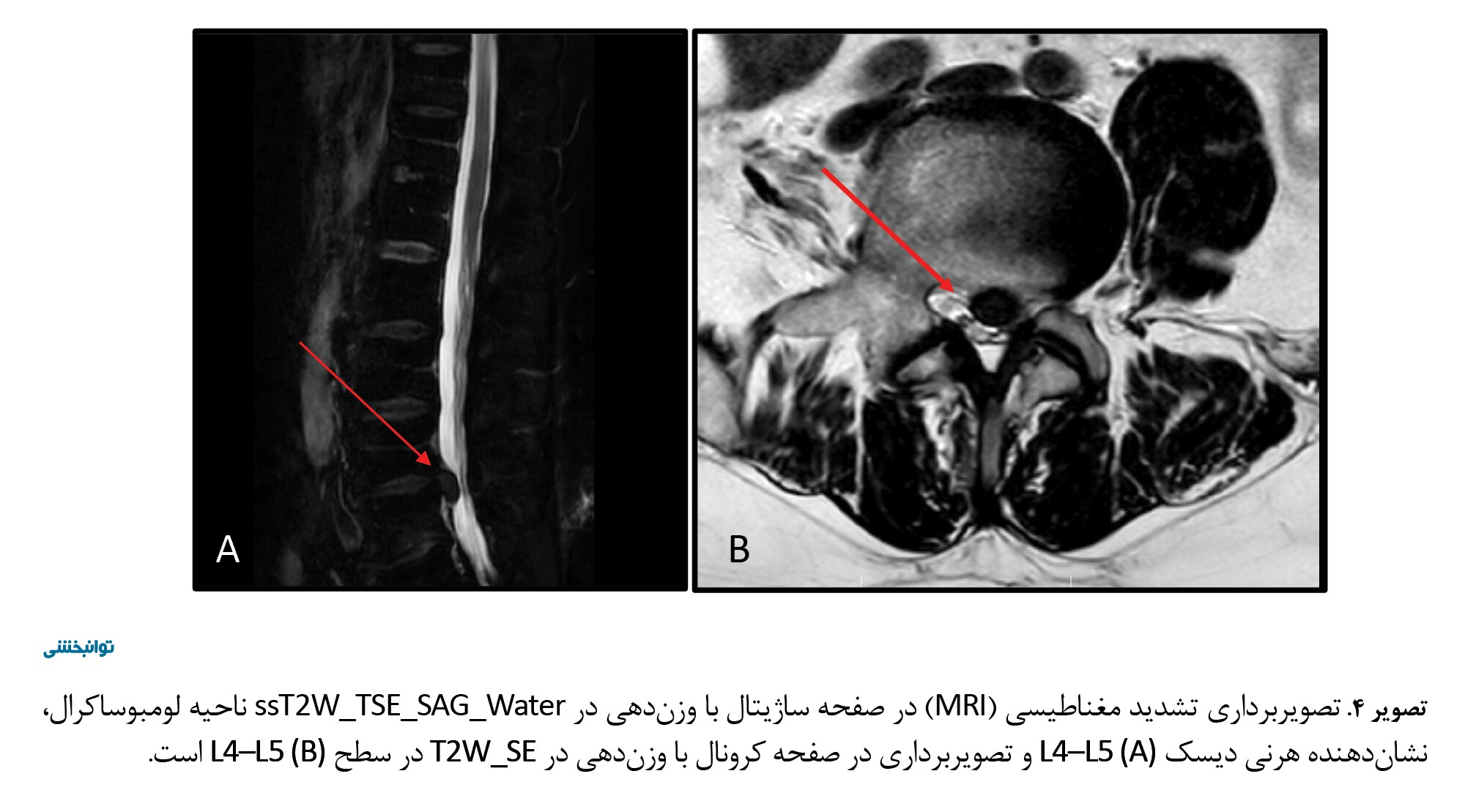
بحث
استئوآرتریت ران بیماری بسیار شایعی است که بزرگسالان را درگیر میکند [۱۰]. اگرچه توزیع جغرافیایی این بیماری متفاوت است، اما برآورد میشود که 25 درصد از افراد مبتلا علائم آن را تجربه میکنند و احتمال انجام تعویض مفصل لگن 10 درصد است [۱۱]. با وجود موفقیت کلی این مداخله، ممکن است به عوارضی مانند فرونشینی ساقه، عفونتها، بیماری ترومبوآمبولی وریدی، آسیبهای عصبی/عروقی، استخوانسازی هتروتوپیک، نابرابری طول پا، شکستگیهای پیرامون پروتز، یا آتروفی عضلانی در اندام مداخلهشده منجر شود که نتیجه آن تغییرات در بیومکانیک لومبوپلویک است [۱۲، ۱۳]. راش و همکاران در مطالعه خود در سال ۲۰۰۷ گزارش کردند که چگونه ۲۲ بیمار مبتلا به آرتروز ران که تحت جراحی قرار گرفتند، دچار تغییراتی در عضلات اندامهای تحتانی شدند که از طریق MRI قابلمشاهده بود و با اختلال عملکرد و درد همراه بود [۱۴]. همراستا با این یافته، ماک و همکاران گزارشی از ۳۴۱ مورد تعویض مفصل ران را منتشر کردند که در آن آتروفی عضله پسواس در سمت جراحی وجود داشت [۷] که با ۴۰ مورد گزارششده در سال ۲۰۱۱ توسط پلومی و همکاران همخوانی دارد [۱۵]. دومی نشان داد که درجه بالاتری از آتروفی یکطرفه و نفوذ چربی بر روی ایمپلنت نسبت به سمت غیرمداخلهشده وجود دارد.
در زمینه جراحی پروتز ران، تنیتومی عضله پسواس در حین کاهش دررفتگی ران، آسیب عصب فمورال ناشی از عمل جراحی [۱۶]، هماتومهای داخل عضلانی، بلند شدن طول اندامهای تحتانی و تحریک عضلانی یا تاندینوپاتی ثانویه به اصطکاک با استابولوم [۱۷] از جمله رویدادهایی هستند که رابطه مستقیمی با آتروفی تدریجی عضله پکتینئوس دارند.
منشأ عضله پسواس در جسمهای مهرهای و دیسکهای بینمهرهای مهرههای T12 ،L1 ،L2 ،L3 و L4 تأثیر تثبیتکننده طبیعی بر روی ستون فقرات دارد و انتقال صحیح نیروهای کرانیوکودال در ناحیه فوقانی کمر را تضمین میکند. بنابراین، در سطوح کمری L4–L5 و L5–S1، تأثیر تثبیتکننده عضله پسواس وجود ندارد. عدم وجود حفاظت طبیعی در نواحی کمری پایین، همراه با افزایش تحرک و بار در این نواحی، ممکن است نقش پیشزمینهای در توسعه پاتولوژیهای انحطاط دیسکهای بینمهرهای در نواحی مهرهای L4-L5 و L5-S1 ایفا کند. این یافته، همراه با دلایل دیگری مانند افزایش تدریجی بار بر روی مهرههای پایین، شواهدی را پشتیبانی میکند که 97 درصد از فتق دیسکها در افراد سالم در دو سطح آخر بینمهرهای بروز میکند، بهطوریکه 54 درصد در سطح L5–S1 و 43 درصد در سطح L4–L5 مشاهده میشود [۱۸]. آتروفی یکطرفه عضله پسواس میتواند به چرخش مزمن لگن منجر شود. این موضوع تمامیت مفاصل ساکروایلیاک و مفاصل بینمهرهای ستون فقرات کمری و مفصل لومبوساکرال را تحت تأثیر قرار میدهد و باعث افزایش گودی کمر و ایجاد تغییرات دژنراتیو در نواحی پایینتر مهرهها میشود [۱۹].
توانبخشی در بیماران تحت عمل تعویض مفصل ران بر دستیابی به بیشترین دامنه حرکتی مفصل بدون درد و کسب الگوی حرکتی عملکردی تمرکز دارد [۲۰]. بااینحال، در این زمینه، باید بر تقویت خم شدن و نزدیک شدن به سمت داخل ران بهطور سیستماتیک تأکید شود و از تغییرات احتمالی در بیومکانیک لومبوپلویک اجتناب گردد. در مورد توصیفشده در این مقاله، درمان توانبخشی استاندارد بلافاصله پس از عمل تعویض مفصل هیپ ران انجام شد و بر بازگرداندن تحرک مفصل ران و دستیابی به بهبودی عملکردی کافی تمرکز داشت. سالها بعد، زمانی که لومبوسیاتیک، آتروفی یکطرفه عضله پسواس و درجه نفوذ چربی شناسایی شد، کار خاصی بر روی عضلات پسواس، لگن و شکم انجام شد تا درد ناشی از بیماری دژنراتیو کمری کاهش یابد.
تحلیل شاخصهای سطح مقطع عضله پسواس در ارتباط با دیسک بینمهرهای L4–L5 مقادیر 0/49 برای سمت راست و 0/99 برای سمت چپ را نشان داد. این یافتهها نشاندهنده اختلاف قابلتوجهی بین دو سمت است که در زمینه بالینی به سمت غیرمؤثر تمایل دارد [۷، ۲۱]. این شاخصها که توسط کیجیما و همکاران استفاده شدهاند، برای ارتباط آتروفی با درد در بیماران مبتلا به ککسارتروز به کار رفته و رابطه واضحی بین درجه آتروفی و وجود درد را نشان میدهند [۲۲].
در مطالعه حاضر آتروفی شدید یکطرفه در سمت راست بهعنوان عامل احتمالی مؤثر در دژنراسیون دیسک و توسعه بعدی لومبوسیاتیک شناسایی شد. این فرآیند احتمالاً در یک دوره میانمدت تا بلندمدت بروز میکند، زیرا بیمار ۸ سال پس از عمل جراحی ران برای درد ناحیه تحتانی کمر به دنبال درمان پزشکی بود.
آتروفی عضله پسواس میتواند بهطور قابلتوجهی بر ثبات ستون فقرات کمری تأثیر بگذارد، بهویژه در بخشهای مهرهای L4–L5–S1 که اهمیت ارزیابی بیومکانیک کمری در طول زمان را در بیماران تحت عمل تعویض مفصل ران تأکید میکند. این ارزیابی مداوم برای درک و رسیدگی به تأثیرات بالقوه آتروفی عضلات بر سلامت و ثبات بلندمدت این بیماران در ناحیه کمری بسیار حیاتی است.
در این زمینه، در نظر گرفتن اطلاعات موجود در مطالعات قبلی که به بررسی بهبود درد کمر پس از عمل تعویض مفصل ران پرداختهاند، حائز اهمیت است. با وجود برخی گزارشها از نرخهای بهبودی که بین 53 تا 82 درصد متغیر است [23-25]، ضروری است توجه داشته باشیم که این مطالعات دارای دوره پیگیری نسبتاً کوتاهی، معمولاً کمتر از ۱ یا ۲ سال بودند. این وضعیت سؤالاتی را درباره پیشرفت واقعی درد ناحیه تحتانی کمر در بیماران پس از عمل تعویض مفصل ران مطرح میکند و بر لزوم تحقیقات بلندمدت با حجم نمونه بزرگ و روشهای با کیفیت بالا تأکید میکند تا بهطور کامل تأثیر این مداخله بر سلامت ستون فقرات کمری را درک کنیم.
ایجاد یک فتق دیسک در سطح بالاتر، تأکید بیشتری بر بروز بالینی این وضعیت میکند. این رویداد میتواند به «بیماری بخش مجاور» در موارد فیوژن مهرهای تشبیه شود [۲۶، ۲۷] و در مورد ما، بهدلیل محدودیت حرکتی در L5-S1 ناشی از دیسکتومی قبلی ایجاد میشود. در این مورد، پس از عمل دیسکتومی L5، یک فتق دیسک پسترولترال چپ L4 ظاهر شد که یک سطح بالاتر است. این رویداد همچنین ارتباط بالقوه بین تغییرات بیومکانیکی کمری و احتمال آتروفی عضله پسواس پس از عمل تعویض مفصل ران را تقویت میکند.
نتیجهگیری
مورد مطرحشده ما را به این فکر میاندازد که عمل تعویض کامل مفصل ران ممکن است به آتروفی یکطرفه طولانیمدت عضله پسواس در سمت همان طرف منجر شود. این واقعیت میتواند بیومکانیک کمری را تغییر دهد و احتمالاً فرآیند انحطاط دیسک و درد کمری بعدی را تسریع کند.
درنهایت، این مطالعه بر نیاز به همکاری نزدیک بین جراحان ارتوپدی، فیزیوتراپیستها، پزشکان توانبخشی و جراحان مغز و اعصاب برای یک رویکرد چندرشتهای و جامع در مدیریت بیماران تحت عمل تعویض مفصل ران تأکید میکند. پیشگیری و شناسایی زودهنگام آتروفی عضله پسواس و مدیریت مناسب آن میتواند بهطور قابلتوجهی روند بالینی و کیفیت زندگی این بیماران را بهبود بخشد و دیدگاههای جدیدی برای پزشکی ارتوپدی و توانبخشی فراهم کند.
بااینحال، دامنه این مطالعه محدود است و سؤالات جدیدی را مطرح میکند. تحقیقات بیشتری لازم است تا رابطه بین آتروفی عضله پسواس، جراحی ران و انحطاط دیسک کمری را روشن کند. مطالعات آینده میتوانند به روشن شدن زمینههای ناشناخته کمک کرده و به توسعه استراتژیهای درمانی دقیقتر و شخصیسازی شده برای بیماران مبتلا کمک کنند.
ملاحظات اخلاقی
پیروی از اصول اخلاق پژوهش
این تحقیق توسط CEICA (کمیته اخلاق تحقیقات بالینی آراگون) با شماره مرجع C.P.-C.I.-PI21/346 تایید شده است.
حامی مالی
این پژوهش هیچگونه کمک مالی از سازمانیهای دولتی، خصوصی و غیرانتفاعی دریافت نکرده است.
مشارکت نویسندگان
تمام نویسندگان در آمادهسازی این مقاله مشارکت داشتند.
تعارض منافع
بنابر اظهار نویسندگان، این مقاله تعارض منافع ندارد.
تشکر و قدردانی
نویسندگان از گروه تحقیقاتی آیهلثی (iHealthy) برای حمایت و همکاری آنها در این پروژه صمیمانه تشکر میکنند.
درد ناحیه کمری بسیار شایع است و یکی از علل اصلی ناتوانی کاری در جوانان به شمار میرود. برآورد میشود که دوسوم بزرگسالان در مقطعی از زندگی خود درد ناحیه تحتانی کمر (LBP) را تجربه میکنند و ۱۰ درصد از آنها به درد ناحیه تحتانی کمر مزمن مبتلا خواهند شد [۱]. یکی از شایعترین علل درد ناحیه تحتانی کمر، انحطاط دیسک بین مهرهای است. عوامل متعددی باعث انحطاط دیسک بین مهرهای میشوند و در بیشتر موارد فعالیتهای شغلی و سبک زندگی، بهویژه عواملی مانند چاقی و سیگار در این زمینه نقش دارند [۲]. روند پیری ازنظر فیزیولوژیکی به انحطاط دیسک بین مهرهای کمک میکند. تخمین زده میشود که در سن ۷۰ سالگی، محتوای آب هسته پالپوزوس تا ۷۰ درصد کاهش مییابد [۳]. سایر عواملی که روند انحطاط را تسریع میکنند عبارتاند از بیماریهای عفونی، فرآیندهای التهابی، تروما یا تغییرات بیومکانیکی [۲، ۴]. علاوهبر عوامل ذکر شده ، تغییرات در عملکرد عضلانی و عوامل بیومکانیکی نقش مهمی در ایجاد و تشدید درد ناحیه تحتانی کمر دارند [۵]. کاستیهای موجود در قدرت و هماهنگی عضلات ممکن است به الگوهای بارگذاری غیرطبیعی بر روی ستون فقرات کمک کنند که این امر فرآیندهای انحطاط را تشدید کرده و خطر ابتلا به درد ناحیه تحتانی کمر را افزایش میدهد [۶].
درک تعامل پیچیده موجود بین عوامل بیومکانیکی و عملکرد عضلات در درد ناحیه تحتانی کمر نقش مهمی در شناخت شرایط مرتبط، مانند عوارض احتمالی تعویض مفصل کامل ران دارد. مطالعات اخیر نشان میدهند که بین تعویض کامل مفصل ران (THA) و آتروفی یکطرفه عضله پسوآس (PM) در سمت ایمپلنت ارتباطی وجود دارد که نشاندهنده این است که این آتروفی احتمالاً عارضه دیرهنگام جراحی باشد [۷]. محل عضله پسوآس آن را به یک تثبیتکننده مهم ستون فقرات تبدیل میکند که بر وضعیت استاتیک و پویایی ستون فقرات کمری تأثیر میگذارد [۸، ۹]. آتروفی عضله پسوآس بهطور قابلتوجهی بر بیومکانیک ستون فقرات کمری تأثیر میگذارد و ممکن است در ایجاد بیماریهای انحطاط دیسک نقش داشته باشد.
در این زمینه، مقاله حاضر مورد بالینی مرد ۵۳ سالهای را که قبلاً تحت درمان تعویض کامل مفصل ران راست قرار گرفته بود، ارائه میکند. 8 سال پس از جراحی، بیمار به وضعیت مزمن Lumbo-sciatalgia دچار شد که پای چپ را تحت تأثیر قرار میداد و همچنین ضعف در خم شدن ران راست را منجر میشد. تحلیلهای بالینی و رادیولوژیک وجود فتق دیسک L5–S1 بیرون برآمده شده و آتروفی یکطرفه عضله پسوآس در همان سمت تعویض مفصل را نشان داد.
درحالیکه بیمار با رویکرد دارویی و توانبخشی محافظهکارانه بهبود یافت، بهبودی کامل، احتمالاً بهدلیل طولانی شدن دوره بهبودی وضعیت وی حاصل نشد. این بهبودی طولانیمدت میتوانست آسیبهای جبرانناپذیری به ساختارهای آناتومیکی آسیبدیده وارد کند و توانایی بیمار را برای بهبودی کامل محدود کند. این مقاله به بررسی مورد بالینی خواهد پرداخت، ارتباط بین آتروفی عضله پسوآس و تحلیل دیسک لومباری را بررسی کرده و بر اهمیت تشخیص زودهنگام و مدیریت جامع در بیماران مبتلا به آتروفی عضله پسوآس پس از تعویض مفصل کامل لگن ران تأکید خواهد کرد.
گذشته از ارائه مورد منحصربهفرد، این مورد بالینی بهعنوان نقطه شروع یک تلاش تحقیقاتی درحالانجام عمل کرده و ارزش آن را در حوزه پزشکی و عمل بالینی روزمره، بهویژه در توانبخشی، مورد تأکید قرار میدهد.
مورد بالینی
مردی ۵۳ ساله با درد حاد عصب سیاتیک چپ به واحد خدمات اورژانس بیمارستان کلینیک دانشگاه لوزانو بلسا مراجعه کرد. او در ۱۲ ساعت گذشته قبل از رسیدن به بخش اورژانس از این درد رنج میبرد و شدت آن در مقیاس عددی ۹ از ۱۰ ارزیابی شده بود. بیمار هرگونه سابقه درد ناحیه تحتانی کمر یا انتشار درد به پا قبل از مراجعه را رد کرد. این درد مکانیکی به اندام تحتانی چپ منتشر میشد که به مچ پا و انگشت شست پا گسترش مییافت. بیمار در زمان پذیرش علائم تب نداشت و اخیراً ترومایی را تجربه نکرده بود. کشش رادیکولار و آزمایشهای مثبت لازگ و براگارد درد را تشدید کرد. معاینه فیزیکی بیشتر نشان داد که بیمار درد در عضلات چهارگوش کمری و عضلات راستکننده ستون فقرات داشت و درد از پشت پا به سمت پا منتشر میشد.
ضعف حرکتی ۲ از ۵ در سیستم درجهبندی عضلانی کندال در اکستنشین انگشت شست پای چپ و در فلکسیون پلانتار مچ پای چپ مشاهده شد. همچنین ضعف متوسط ۲ از ۵ در فلکسیون ران راست وجود داشت و سایر میوتومهای lumbosacral طبیعی بودند. معاینه حسی نشان داد در درماتوم S1 سمت چپ هیپوستزی و هیپوآلژزی وجود دارد، اما در سایر درماتومها تغییری مشاهده نشد. هیچ اختلال حسی مرتبط با cauda equina مشاهده نشد و نشانهای از اختلال عملکرد اسفنکتر تشخیص داده نشد.
شرح حال و ارزیابی رادیولوژیکی
با بررسی سابقه پزشکی بیمار، متوجه شدیم که او در آوریل ۲۰۱۲ بهدلیل ککسارتروز تکطرفه پیشرفته در طی 2 سال گذشته، عمل تعویض مفصل ران راست را انجام داده است و 4 هفته پس از جراحی، بیمار 6 جلسه فیزیوتراپی را انجام داد. در این جلسات به بیمار آموزش داده شد و ارزیابی شد که چگونه علاوهبر بازآموزی راه رفتن، تمرینات تقویت عضلانی برای لگن (عضلات گلوتئال، ایلیوپسوآس، ادکتورها، چهارسر ران و همسترینگها) را انجام دهد. بیمار از ضعف خفیف در فلکسیون لگن راست و درد در ناحیه کشاله ران راست گزارش داد، اما هیچ دردی در ناحیه کمری وجود نداشت. این علائم بهعنوان عوارض شایع پس از جراحی در نظر گرفته شد. عمل تعویض مفصل ران که از طریق رویکرد جانبی با پروتز SL-Plus+Epfit انجام شد، بهعنوان پاسخ به استئوآرتریت لگن درجه ۳ طبق طبقهبندی کِلگرن–لارنس (تصویر شماره ۱) نشان داده شد.

شاخص توده بدنی 29/58 کیلوگرم بر مترمربع بود. اشعه ایکس ناحیه کمری نتایج قابلتوجهی را نشان نداد، اما تصویربرداری تشدید مغناطیسی (MRI) ناحیه کمری وجود فتق دیسک پارامدین چپ در سطح L5–S1 را نشان داد که با قطعهای از دیسک بینمهرهای حجیم که از محل اصلی خود جدا شده بود در extraforaminal همراه بود (تصویر شماره 2).

آتروفی قابلتوجهی از عضله پسوآس راست مشخص بود و با نفوذ بافت چربی در همان ناحیه تشدید شده بود. مساحت مقطع عرضی (CSA) عضله پسوآس بهطور دوطرفه توسط یک رادیولوژیست در دیسک بینمهرهای L3–L4 اندازهگیری شد و مساحتی معادل ۶۸۱ میلیمتر مربع در سمت راست بهدست آمد که نمره گوتالیه ۳ نشاندهنده آتروفی شدید عضلانی بود. سمت چپ مساحتی معادل ۱۳۸۸ میلیمتر مربع داشت و نمره گوتالیه صفر بود (تصویر شماره ۳ الف). شاخصهای مساحت مقطع عرضی عضله پسواس/دیسک در سمت راست و چپ بهترتیب 0/49 و 0/99 محاسبه شد. تصویربرداری، تشدید مغناطیسی بخشهایی از عضله پسوآس بدون شکم عضلانی را نشان داد (تصویر شماره ۳ ب). این یافتهها آسیبشناسی را نشان دادند و بیماریهای دیگر عصبی-عضلانی و بیماریهای سیستم عصبی مرکزی را رد کردند.

بهبود
بهدلیل شدت درد و تظاهرات بالینی، بیمار در بخش جراحی مغز و اعصاب بستری شد و تحت درمان با داروهای ضددرد مشتق از مواد افیونی (مسکنهای قوی) قرار گرفت. علاوهبراین، تزریق اپیدورال دمی با بیحسکننده موضعی و کورتیکواستروئید انجام شد که به پاسخ مطلوب منجر شد. بیمار پس از 2 روز بستری شدن ترخیص شد و یک برنامه توانبخشی از طریق ۱۵ جلسه فیزیوتراپی با تمریناتی که بر تقویت عضلات خمکننده سمت راست لگن متمرکز بود، آغاز گردید. در این برنامه بهویژه به عضله پسواس، تمرینات تثبیتکننده لومبوپلویک، کششهای عضلات راستکننده کمر، تحریک الکتریکی عصب از راه پوست برای تسکین درد و دینامیک عصبی عصب سیاتیک توجه ویژهای شد. بازآموزی راه رفتن نیز بخشی اساسی از برنامه درمانی بود که به اصلاح الگوهای غیرطبیعی ضددرد و بهبود دینامیک حرکتی کمک کرد. یک الکترومیوگرام که بهصورت سرپایی انجام شد، الگوی مزمن رادیکولار رنج و دنوورهسازی ریشه چپ S1 را نشان داد.
علیرغم تلاشهای مداوم در درمان محافظه کارانه و توانبخشی، تداوم درد و درگیری رادیکولار به مرحله جدیدی از درمان منجر شد. باتوجهبه مدت طولانی علائم که حدود ۲۴ ماه به طول انجامید و عدم پاسخ رضایتبخش به اقدامات غیرجراحی، مداخله جراحی در فوریه ۲۰۲۱ ضروری بود. درنهایت، جراحی از طریق میکرو دیسککتومی و فارامینوتومی چپ L5–S1 انجام شد که بهطور موفقیتآمیزی درد را بهمدت حدود ۱۲ ماه تسکین داد. 1 سال بعد، بیمار دوباره با رادیکولاپاتی چپ L5 بدون نقص حسی یا حرکتی مراجعه کرد. آخرین MRI ناحیه کمری، فتق دیسک میدیوپارامدیکال و پستولترال سمت چپ در سطح L4–L5 را نشان داد. این فتق بالاتر از فتق دیسکی که قبلاً درمانشده بود قرار داشت که همراه با حرکت مختصر caudal که با ریشه چپ L5 تماس قابلتوجه و وسیعی داشت بود (تصویر شماره ۴). باتوجهبه یافتههای درد رادیکولار چپ L5 بدون نقص عصبی در نواحی دورتر از ناحیه آسیبدیده در آخرین معاینه فیزیکی، بیمار تحت نظر بخش مدیریت و درمان درد برای ارزیابی و مدیریت بیشتر قرار گرفت.

بحث
استئوآرتریت ران بیماری بسیار شایعی است که بزرگسالان را درگیر میکند [۱۰]. اگرچه توزیع جغرافیایی این بیماری متفاوت است، اما برآورد میشود که 25 درصد از افراد مبتلا علائم آن را تجربه میکنند و احتمال انجام تعویض مفصل لگن 10 درصد است [۱۱]. با وجود موفقیت کلی این مداخله، ممکن است به عوارضی مانند فرونشینی ساقه، عفونتها، بیماری ترومبوآمبولی وریدی، آسیبهای عصبی/عروقی، استخوانسازی هتروتوپیک، نابرابری طول پا، شکستگیهای پیرامون پروتز، یا آتروفی عضلانی در اندام مداخلهشده منجر شود که نتیجه آن تغییرات در بیومکانیک لومبوپلویک است [۱۲، ۱۳]. راش و همکاران در مطالعه خود در سال ۲۰۰۷ گزارش کردند که چگونه ۲۲ بیمار مبتلا به آرتروز ران که تحت جراحی قرار گرفتند، دچار تغییراتی در عضلات اندامهای تحتانی شدند که از طریق MRI قابلمشاهده بود و با اختلال عملکرد و درد همراه بود [۱۴]. همراستا با این یافته، ماک و همکاران گزارشی از ۳۴۱ مورد تعویض مفصل ران را منتشر کردند که در آن آتروفی عضله پسواس در سمت جراحی وجود داشت [۷] که با ۴۰ مورد گزارششده در سال ۲۰۱۱ توسط پلومی و همکاران همخوانی دارد [۱۵]. دومی نشان داد که درجه بالاتری از آتروفی یکطرفه و نفوذ چربی بر روی ایمپلنت نسبت به سمت غیرمداخلهشده وجود دارد.
در زمینه جراحی پروتز ران، تنیتومی عضله پسواس در حین کاهش دررفتگی ران، آسیب عصب فمورال ناشی از عمل جراحی [۱۶]، هماتومهای داخل عضلانی، بلند شدن طول اندامهای تحتانی و تحریک عضلانی یا تاندینوپاتی ثانویه به اصطکاک با استابولوم [۱۷] از جمله رویدادهایی هستند که رابطه مستقیمی با آتروفی تدریجی عضله پکتینئوس دارند.
منشأ عضله پسواس در جسمهای مهرهای و دیسکهای بینمهرهای مهرههای T12 ،L1 ،L2 ،L3 و L4 تأثیر تثبیتکننده طبیعی بر روی ستون فقرات دارد و انتقال صحیح نیروهای کرانیوکودال در ناحیه فوقانی کمر را تضمین میکند. بنابراین، در سطوح کمری L4–L5 و L5–S1، تأثیر تثبیتکننده عضله پسواس وجود ندارد. عدم وجود حفاظت طبیعی در نواحی کمری پایین، همراه با افزایش تحرک و بار در این نواحی، ممکن است نقش پیشزمینهای در توسعه پاتولوژیهای انحطاط دیسکهای بینمهرهای در نواحی مهرهای L4-L5 و L5-S1 ایفا کند. این یافته، همراه با دلایل دیگری مانند افزایش تدریجی بار بر روی مهرههای پایین، شواهدی را پشتیبانی میکند که 97 درصد از فتق دیسکها در افراد سالم در دو سطح آخر بینمهرهای بروز میکند، بهطوریکه 54 درصد در سطح L5–S1 و 43 درصد در سطح L4–L5 مشاهده میشود [۱۸]. آتروفی یکطرفه عضله پسواس میتواند به چرخش مزمن لگن منجر شود. این موضوع تمامیت مفاصل ساکروایلیاک و مفاصل بینمهرهای ستون فقرات کمری و مفصل لومبوساکرال را تحت تأثیر قرار میدهد و باعث افزایش گودی کمر و ایجاد تغییرات دژنراتیو در نواحی پایینتر مهرهها میشود [۱۹].
توانبخشی در بیماران تحت عمل تعویض مفصل ران بر دستیابی به بیشترین دامنه حرکتی مفصل بدون درد و کسب الگوی حرکتی عملکردی تمرکز دارد [۲۰]. بااینحال، در این زمینه، باید بر تقویت خم شدن و نزدیک شدن به سمت داخل ران بهطور سیستماتیک تأکید شود و از تغییرات احتمالی در بیومکانیک لومبوپلویک اجتناب گردد. در مورد توصیفشده در این مقاله، درمان توانبخشی استاندارد بلافاصله پس از عمل تعویض مفصل هیپ ران انجام شد و بر بازگرداندن تحرک مفصل ران و دستیابی به بهبودی عملکردی کافی تمرکز داشت. سالها بعد، زمانی که لومبوسیاتیک، آتروفی یکطرفه عضله پسواس و درجه نفوذ چربی شناسایی شد، کار خاصی بر روی عضلات پسواس، لگن و شکم انجام شد تا درد ناشی از بیماری دژنراتیو کمری کاهش یابد.
تحلیل شاخصهای سطح مقطع عضله پسواس در ارتباط با دیسک بینمهرهای L4–L5 مقادیر 0/49 برای سمت راست و 0/99 برای سمت چپ را نشان داد. این یافتهها نشاندهنده اختلاف قابلتوجهی بین دو سمت است که در زمینه بالینی به سمت غیرمؤثر تمایل دارد [۷، ۲۱]. این شاخصها که توسط کیجیما و همکاران استفاده شدهاند، برای ارتباط آتروفی با درد در بیماران مبتلا به ککسارتروز به کار رفته و رابطه واضحی بین درجه آتروفی و وجود درد را نشان میدهند [۲۲].
در مطالعه حاضر آتروفی شدید یکطرفه در سمت راست بهعنوان عامل احتمالی مؤثر در دژنراسیون دیسک و توسعه بعدی لومبوسیاتیک شناسایی شد. این فرآیند احتمالاً در یک دوره میانمدت تا بلندمدت بروز میکند، زیرا بیمار ۸ سال پس از عمل جراحی ران برای درد ناحیه تحتانی کمر به دنبال درمان پزشکی بود.
آتروفی عضله پسواس میتواند بهطور قابلتوجهی بر ثبات ستون فقرات کمری تأثیر بگذارد، بهویژه در بخشهای مهرهای L4–L5–S1 که اهمیت ارزیابی بیومکانیک کمری در طول زمان را در بیماران تحت عمل تعویض مفصل ران تأکید میکند. این ارزیابی مداوم برای درک و رسیدگی به تأثیرات بالقوه آتروفی عضلات بر سلامت و ثبات بلندمدت این بیماران در ناحیه کمری بسیار حیاتی است.
در این زمینه، در نظر گرفتن اطلاعات موجود در مطالعات قبلی که به بررسی بهبود درد کمر پس از عمل تعویض مفصل ران پرداختهاند، حائز اهمیت است. با وجود برخی گزارشها از نرخهای بهبودی که بین 53 تا 82 درصد متغیر است [23-25]، ضروری است توجه داشته باشیم که این مطالعات دارای دوره پیگیری نسبتاً کوتاهی، معمولاً کمتر از ۱ یا ۲ سال بودند. این وضعیت سؤالاتی را درباره پیشرفت واقعی درد ناحیه تحتانی کمر در بیماران پس از عمل تعویض مفصل ران مطرح میکند و بر لزوم تحقیقات بلندمدت با حجم نمونه بزرگ و روشهای با کیفیت بالا تأکید میکند تا بهطور کامل تأثیر این مداخله بر سلامت ستون فقرات کمری را درک کنیم.
ایجاد یک فتق دیسک در سطح بالاتر، تأکید بیشتری بر بروز بالینی این وضعیت میکند. این رویداد میتواند به «بیماری بخش مجاور» در موارد فیوژن مهرهای تشبیه شود [۲۶، ۲۷] و در مورد ما، بهدلیل محدودیت حرکتی در L5-S1 ناشی از دیسکتومی قبلی ایجاد میشود. در این مورد، پس از عمل دیسکتومی L5، یک فتق دیسک پسترولترال چپ L4 ظاهر شد که یک سطح بالاتر است. این رویداد همچنین ارتباط بالقوه بین تغییرات بیومکانیکی کمری و احتمال آتروفی عضله پسواس پس از عمل تعویض مفصل ران را تقویت میکند.
نتیجهگیری
مورد مطرحشده ما را به این فکر میاندازد که عمل تعویض کامل مفصل ران ممکن است به آتروفی یکطرفه طولانیمدت عضله پسواس در سمت همان طرف منجر شود. این واقعیت میتواند بیومکانیک کمری را تغییر دهد و احتمالاً فرآیند انحطاط دیسک و درد کمری بعدی را تسریع کند.
درنهایت، این مطالعه بر نیاز به همکاری نزدیک بین جراحان ارتوپدی، فیزیوتراپیستها، پزشکان توانبخشی و جراحان مغز و اعصاب برای یک رویکرد چندرشتهای و جامع در مدیریت بیماران تحت عمل تعویض مفصل ران تأکید میکند. پیشگیری و شناسایی زودهنگام آتروفی عضله پسواس و مدیریت مناسب آن میتواند بهطور قابلتوجهی روند بالینی و کیفیت زندگی این بیماران را بهبود بخشد و دیدگاههای جدیدی برای پزشکی ارتوپدی و توانبخشی فراهم کند.
بااینحال، دامنه این مطالعه محدود است و سؤالات جدیدی را مطرح میکند. تحقیقات بیشتری لازم است تا رابطه بین آتروفی عضله پسواس، جراحی ران و انحطاط دیسک کمری را روشن کند. مطالعات آینده میتوانند به روشن شدن زمینههای ناشناخته کمک کرده و به توسعه استراتژیهای درمانی دقیقتر و شخصیسازی شده برای بیماران مبتلا کمک کنند.
ملاحظات اخلاقی
پیروی از اصول اخلاق پژوهش
این تحقیق توسط CEICA (کمیته اخلاق تحقیقات بالینی آراگون) با شماره مرجع C.P.-C.I.-PI21/346 تایید شده است.
حامی مالی
این پژوهش هیچگونه کمک مالی از سازمانیهای دولتی، خصوصی و غیرانتفاعی دریافت نکرده است.
مشارکت نویسندگان
تمام نویسندگان در آمادهسازی این مقاله مشارکت داشتند.
تعارض منافع
بنابر اظهار نویسندگان، این مقاله تعارض منافع ندارد.
تشکر و قدردانی
نویسندگان از گروه تحقیقاتی آیهلثی (iHealthy) برای حمایت و همکاری آنها در این پروژه صمیمانه تشکر میکنند.
References
- Domenech J, Baños R, Peñalver L, Garcia-Palacios A, Herrero R, Ezzedine A, et al. Design considerations of a randomized clinical trial on a cognitive behavioural intervention using communication and information technologies for managing chronic low back pain. BMC Musculoskeletal Disorders. 2013; 14:142. [DOI:10.1186/1471-2474-14-142] [PMID]
- Oichi T, Taniguchi Y, Oshima Y, Tanaka S, Saito T. Pathomechanism of intervertebral disc degeneration. JOR Spine. 2020; 3(1):e1076. [DOI:10.1002/jsp2.1076] [PMID]
- Buckwalter JA. Aging and degeneration of the human intervertebral disc. Spine (Phila Pa 1976). 1995; 20(11):1307-14. [DOI:10.1097/00007632-199506000-00022] [PMID]
- Kos N, Gradisnik L, Velnar T. A brief review of the degenerative intervertebral disc disease. Medical Archives. 2019; 73(6):421-4. [DOI:10.5455/medarh.2019.73.421-424] [PMID]
- Noonan AM, Brown SHM. Paraspinal muscle pathophysiology associated with low back pain and spine degenerative disorders. JOR Spine. 2021; 4(3):e1171. [DOI:10.1002/jsp2.1171] [PMID]
- Alston W, Carlson KE, Feldman DJ, Grimm Z, Gerontinos E. A quantitative study of muscle factors in the chronic low back syndrome. Journal of the American Geriatrics Society. 1966; 14(10):1041-7. [DOI:10.1111/j.1532-5415.1966.tb02885.x] [PMID]
- Mak D, Chisholm C, Davies AM, Botchu R, James SL. Psoas muscle atrophy following unilateral hip arthroplasty. Skeletal Radiology. 2020; 49(10):1539-45. [DOI:10.1007/s00256-020-03447-3] [PMID]
- Syed HR, Yaeger K, Sandhu FA. Resolution of the more anteriorly positioned psoas muscle following correction of spinal sagittal alignment from spondylolisthesis: Case report. Journal of Neurosurgery Spine. 2017; 26(4):441-7. [DOI:10.3171/2016.9.SPINE16324] [PMID]
- Elliott JM, Zylstra ED, Centeno CJ. The presence and utilization of psoas musculature despite congenital absence of the right hip. Manual Therapy. 2004; 9(2):109-13. [DOI:10.1016/S1356-689X(03)00128-0] [PMID]
- Katz JN, Arant KR, Loeser RF. Diagnosis and treatment of hip and knee osteoarthritis: A review. Journal of the American Medical Association. 2021; 325(6):568-78. [DOI:10.1001/jama.2020.22171] [PMID]
- Murphy NJ, Eyles JP, Hunter DJ. Hip osteoarthritis: Etiopathogenesis and implications for management. Advances in Therapy. 2016; 33(11):1921-46. [DOI:10.1007/s12325-016-0409-3] [PMID]
- Nutt JL, Papanikolaou K, Kellett CF. (ii) Complications of total hip arthroplasty. Orthopaedics and Trauma. 2013; 27(5):272-6. [DOI:10.1016/j.mporth.2013.08.012]
- Nolan DR, Fitzgerald RH Jr, Beckenbaugh RD, Coventry MB. Complications of total hip arthroplasty treated by reoperation. The Journal of Bone and Joint Surgery. 1975; 57(7):977-81. [DOI:10.2106/00004623-197557070-00017]
- Rasch A, Byström AH, Dalen N, Berg HE. Reduced muscle radiological density, cross-sectional area, and strength of major hip and knee muscles in 22 patients with hip osteoarthritis. Acta Orthopaedica. 2007; 78(4):505-10. [DOI:10.1080/17453670710014158] [PMID]
- Ploumis A, Michailidis N, Christodoulou P, Kalaitzoglou I, Gouvas G, Beris A. Ipsilateral atrophy of paraspinal and psoas muscle in unilateral back pain patients with monosegmental degenerative disc disease. The British Journal of Radiology. 2011; 84(1004):709-13. [DOI:10.1259/bjr/58136533] [PMID]
- Slater N, Singh R, Senasinghe N, Gore R, Goroszeniuk T, James D. Pressure monitoring of the femoral nerve during total hip replacement: An explanation for iatropathic palsy. Journal of the Royal College of Surgeons of Edinburgh. 2000; 45(4):231-3. [PMID]
- Morohashi I, Homma Y, Kanda A, Yamamoto Y, Obata H, Mogami A, et al. Iliopsoas impingement after revision total hip arthroplasty treated with iliopsoas muscle transection. Annals of Medicine and Surgery. 2016; 7:30-3. [DOI:10.1016/j.amsu.2016.03.004] [PMID]
- Martínez A. [Valoración de la efectividad de Escuela de Espalda en pacientes afectos de lumbalgia subaguda o crónica (Spanish)] [PhD dissertation] . Zaragoza: Universidad de Zaragoza; 2018. [Link]
- Regev GJ, Kim CW, Tomiya A, Lee YP, Ghofrani H, Garfin SR, et al. Psoas muscle architectural design, in vivo sarcomere length range, and passive tensile properties support its role as a lumbar spine stabilizer. Spine (Phila Pa 1976). 2011; 36(26):E1666-74. [DOI:10.1097/BRS.0b013e31821847b3] [PMID]
- Garden FH. Rehabilitation Following total hip arthroplasty. Journal of Back and Musculoskeletal Rehabilitation. 1994; 4(3):185-92. [DOI:10.3233/BMR-1994-4308] [PMID]
- Pezolato A, de Vasconcelos EE, Defino HL, Nogueira-Barbosa MH. Fat infiltration in the lumbar multifidus and erector spinae muscles in subjects with sway-back posture. European Spine Journal. 2012; 21(11):2158-64. [DOI:10.1007/s00586-012-2286-z] [PMID]
- Kijima H, Yamada S, Konishi N, Kubota H, Tazawa H, Tani T, et al. The differences in imaging findings between painless and painful osteoarthritis of the hip. Clinical Medicine Insights Arthritis Musculoskeletal Disorders. 2020; 13:117954412094674. [DOI:10.1177/1179544120946747] [PMID]
- Parvizi J, Pour AE, Hillibrand A, Goldberg G, Sharkey PF, Rothman RH. Back pain and total hip arthroplasty: A prospective natural history study. Clinical Orthopaedics and Related Research. 2010; 468(5):1325-30. [DOI:10.1007/s11999-010-1236-5] [PMID]
- Vigdorchik JM, Shafi KA, Kolin DA, Buckland AJ, Carroll KM, Jerabek SA. Does low back pain improve following total hip arthroplasty? The Journal of Arthroplasty. 2022; 37(8):S937-40. [DOI:10.1016/j.arth.2022.03.038] [PMID]
- Staibano P, Winemaker M, Petruccelli D, de Beer J. Total joint arthroplasty and preoperative low back pain. The Journal of Arthroplasty. 2014; 29(5):867-71. [DOI:10.1016/j.arth.2013.10.001] [PMID]
- McDonald CL, Alsoof D, Glueck J, Osorio C, Stone B, McCluskey L, et al. Adjacent segment disease after spinal fusion. JBJS Reviews. 2023; 11(6):e23.00028. [DOI:10.2106/JBJS.RVW.23.00028]
- Park P, Garton HJ, Gala VC, Hoff JT, McGillicuddy JE. Adjacent segment disease after lumbar or lumbosacral fusion: Review of the literature. Spine (Phila Pa 1976). 2004; 29(17):1938-44. [DOI:10.1097/01.brs.0000137069.88904.03] [PMID]
نوع مطالعه: گزارش موردی |
موضوع مقاله:
مدیریت توانبخشی
دریافت: 1402/12/20 | پذیرش: 1403/4/13 | انتشار: 1403/10/12
دریافت: 1402/12/20 | پذیرش: 1403/4/13 | انتشار: 1403/10/12
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |








