دوره 20، شماره 2 - ( تابستان 1398 )
دوره، شماره، فصل و سال، شماره مسلسل |
برگشت به فهرست نسخه ها
Download citation:
BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:



BibTeX | RIS | EndNote | Medlars | ProCite | Reference Manager | RefWorks
Send citation to:
Zarezadeh F, Arazpour M, Bahramizadeh M, Mardani M A. Comparing the Effect of New Silicone Foot Prosthesis and Conventional Foot Prosthesis on Plantar Pressure in Diabetic Patients With Transmetatarsal Amputation. jrehab 2019; 20 (2) :124-135
URL: http://rehabilitationj.uswr.ac.ir/article-1-2576-fa.html
URL: http://rehabilitationj.uswr.ac.ir/article-1-2576-fa.html
زارع زاده فاطمه، عراضپور مختار، بهرامی زاده محمود، مردانی محمدعلی. مقایسه تأثیر پروتز سیلیکونی جدید با پروتز سیلیکونی مرسوم بر نحوه توزیع فشار کفپایی در بیماران دیابتی با آمپوتاسیون ترنسمتاتارسال. مجله توانبخشی. 1398; 20 (2) :124-135
URL: http://rehabilitationj.uswr.ac.ir/article-1-2576-fa.html
1- گروه ارتز و پروتز، دانشگاه علوم بهزیستی و توانبخشی، تهران، ایران.
2- گروه ارتز و پروتز، دانشگاه علوم بهزیستی و توانبخشی، تهران، ایران. ،natelnoory@yahoo.com
2- گروه ارتز و پروتز، دانشگاه علوم بهزیستی و توانبخشی، تهران، ایران. ،
متن کامل [PDF 2883 kb]
(2098 دریافت)
| چکیده (HTML) (5434 مشاهده)
متن کامل: (1732 مشاهده)
مقدمه
دیابت بیماری نسبتاً شایعی است که به مرور زمان عوارض مختلفی ایجاد میکند. یکی از خطرناکترین عوارض دیابت ایجاد زخمهای مزمن در پاست. در حال حاضر 4۰5/۶ میلیون بزرگسال مبتلا به دیابت هستند و تا سال 20۳0 تعداد این افراد به ۵۱۰/۸ میلیون نفر افزایش مییابد [1]. نروپاتی محیطی، افزایش فشار کفپایی، مشکلات عروقی، کمشدن دامنه حرکتی مفاصل، دفرمیتیهای پا، کنترلنکردن قند خون، افزایش سابقه بیماری و افزایش سن، همگی از عوامل ایجادکننده زخمهای مکرر پا و درنهایت قطع عضو هستند [2]. خطر ابتلا به زخم و قطع عضو در افراد مبتلا به دیابت نسبت به افراد غیردیابتی بسیار بیشتر است. برآورد شده است که هر 20 ثانیه یک قطع عضو در فرد مبتلا به دیابت در جایی در جهان انجام میشود [3].
مراقبتهای ارتزی یا پروتزی پس از قطع عضو پارشیال پا در بیماران دیابتی متفاوت است. ارتز یا پروتز ایدئآل در یک فرد مبتلا به دیابت و در معرض خطر قطع عضو مجدد، باید فشار را بر کل سطح پا پراکنده و از ایجاد فشارهای موضعی جلوگیری کند [4]. مواد سیلیکونی میتوانند در ساخت پروتزهای پارشیال پا به کار گرفته شوند. این پروتزها از لحاظ زیبایی بر دیگر پروتزهای استفادهشده برای افراد پارشیال پا برتری دارند. از طرف دیگر استفاده از پروتزهایی که زیبایی بیشتری برای آمپوتههای پارشیال پا فراهم میکنند، بیشتر با درخواست آمپوتهها مواجه است [5]. پروتزهای سیلیکونی جزء پروتزهای انعطافپذیر محسوب میشوند.
سیلیکون، خواص مختلفی دارد که به عنوان بهترین ماده، برای ساخت پروتزهای سیلیکونی شناخته شده است؛ برای مثال، در مقایسه با دیگر موادی که در ساخت پروتزها استفاده میشود، بیشترین اصطکاک را با پوست دارد [6]. این خاصیت، سبب میشود حین استفاده از پروتزهای پارشیال پا که از جنس سیلیکون ساخته شدهاند، پروتز کمترین حرکت را نسبت به پوست داشته باشد. ویژگی بارز دیگری که میتوان برای سیلیکون در نظر گرفت آن است که برخلاف دیگر پلیمرها، که ریشهای نفتی دارند، این ماده، ریشه معدنی دارد (سنگ سیلیکات) و در اثر اختلاف دما، نرم و سخت نمیشود. یعنی دما و دیگر شرایط محیطی، در مقایسه با دیگر مواد، کمترین تغییر را در خواص مکانیکی این پلیمر ایجاد میکند [7].
این ماده در اشکال متنوعی تولید میشود و میتواند در حالت سفت یا برعکس بسیار نرم ساخته شود. زمانی که سیلیکون بسیار نرم تولید میشود، نهتنها پدینگ و نَرمسازی بسیار خوبی ایجاد میکند، بلکه از پوست در برابر سایش و برش نیز محافظت میکند. این نکته میتواند اهمیت زیادی داشته باشد، چون سائیدگی به نوعی مهمترین عامل تخریب پوست و بروز مشکلات پوستی به شمار میآید. در کشورهای صنعتی سازنده ماده اولیه سیلیکون، این ماده با خواص گوناگون و برای مصارف مختلف، تهیه و عرضه میشود و برای ساخت پروتز، نوع Medical grade (که در سختیهای مختلف موجود است) استفاده میشود. بررسی پروتزهای سیلیکونی استفادهشده در این زمینه نشان میدهد پروتزیستها در تمامی موارد از مواد با سختی یکسان در تمام دیوارههای سوکت استفاده میکنند [10-8].
بررسی مطالعات انجامشده در این زمینه نیز نشان داد افزایش درخور توجه فشار در استامپ، بعد از قطع عضو پارشیال پا وجود دارد که این افزایش فشار نیاز به توزیع مناسبتر به صورت ویژه در نقاط پرفشار دارد [12 ،11]. از آنجایی که سوکت پروتزهای سیلیکونی در تمام دیواره سختی یکسان دارد، بالطبع نمیتواند این مشکل را مرتفع کند، بنابراین هدف از انجام این مطالعه در گام نخست، شناسایی نقاط پُرفشار در استامپ حین استفاده از پروتزهای سیلیکونی رایج و در گام دوم استفاده از مواد سیلیکونی با سختی کمتر در نقاط پرفشار و طراحی پروتزی جدید است که باعث توزیع مناسبتر فشار در این افراد شود. به طور کلی هدف ما در این مطالعه طراحی و ساخت پروتز سیلیکونی جدید به منظور کاهش فشارهای موضعی با درنظرگرفتن شرایط استامپ و انتخاب سختیهای مناسب سیلیکون برای این بیماران و درنهایت ارزیابی و مقایسه آن با پروتزهای سیلیکونی مرسوم بود.
روش بررسی
این پژوهش شبهتجربی روی پنج بیمار دیابتی با قطع عضو ترنس متاتارسال (سه زن و دو مرد) در سال 1396 انجام گرفت. نمونهگیری به صورت غیراحتمالی ساده بود و شرکتکنندگان در آزمایشگاه راهرفتن گروه ارتز و پروتز دانشگاه علوم بهزیستی و توانبخشی ارزیابی شدند. ملاکهای ورود به پژوهش عبارت بودند از دیابت نوع ۲، قطع عضو پارشیال پا در سطح ترنسمتاتارسال حداقل در یک اندام که بیش از یک سال از آن گذشته باشد، استفاده از پروتزهای سیلیکونی مرسوم در گذشته حداقل به مدت 3 ماه، توانایی در راهرفتن بدون کمک بیش از 100 متر، نداشتن جراحی اندام تحتانی مانند پروتز هیپ، زانو، مچ و پا، نبود اختلاف طول دو اندام، نداشتن سابقه جراحی یا آسیب به کمر، سن زیر 65 سال، نداشتن زخم در استامپ. ملاکهای خروج از مطالعه نیز ایجاد زخم جدید در استامپ، درد شدید حاصل از نوروما که مانع راهرفتن بیمار شود و تمایلنداشتن بیمار به ادامه همکاری بود [16-13 ،8]. برای جمعآوری اطلاعات از ابزارهایی که در ادامه ذکر شده استفاده شد. دستگاه سنجش فشار کفپایی شرکت ناول آلمان مدل پدار-ایکس برای اندازهگیری فشار کف پایی در طول راهرفتن و شش حسگر سنجش فشار مقاومتی از نوع Force Sensing Resistors (FSR-402, Interlink Electronics) (تصویر شماره ۱). این حسگرها روی نقاطی از استامپ که فشار بیش از ۲۰۰ کیلوپاسکال داشت با چسب ثابت شدند و اطلاعات آنها وارد یک بسته پردازشگر شد که روی ساق قرار گرفته بود.
دیابت بیماری نسبتاً شایعی است که به مرور زمان عوارض مختلفی ایجاد میکند. یکی از خطرناکترین عوارض دیابت ایجاد زخمهای مزمن در پاست. در حال حاضر 4۰5/۶ میلیون بزرگسال مبتلا به دیابت هستند و تا سال 20۳0 تعداد این افراد به ۵۱۰/۸ میلیون نفر افزایش مییابد [1]. نروپاتی محیطی، افزایش فشار کفپایی، مشکلات عروقی، کمشدن دامنه حرکتی مفاصل، دفرمیتیهای پا، کنترلنکردن قند خون، افزایش سابقه بیماری و افزایش سن، همگی از عوامل ایجادکننده زخمهای مکرر پا و درنهایت قطع عضو هستند [2]. خطر ابتلا به زخم و قطع عضو در افراد مبتلا به دیابت نسبت به افراد غیردیابتی بسیار بیشتر است. برآورد شده است که هر 20 ثانیه یک قطع عضو در فرد مبتلا به دیابت در جایی در جهان انجام میشود [3].
مراقبتهای ارتزی یا پروتزی پس از قطع عضو پارشیال پا در بیماران دیابتی متفاوت است. ارتز یا پروتز ایدئآل در یک فرد مبتلا به دیابت و در معرض خطر قطع عضو مجدد، باید فشار را بر کل سطح پا پراکنده و از ایجاد فشارهای موضعی جلوگیری کند [4]. مواد سیلیکونی میتوانند در ساخت پروتزهای پارشیال پا به کار گرفته شوند. این پروتزها از لحاظ زیبایی بر دیگر پروتزهای استفادهشده برای افراد پارشیال پا برتری دارند. از طرف دیگر استفاده از پروتزهایی که زیبایی بیشتری برای آمپوتههای پارشیال پا فراهم میکنند، بیشتر با درخواست آمپوتهها مواجه است [5]. پروتزهای سیلیکونی جزء پروتزهای انعطافپذیر محسوب میشوند.
سیلیکون، خواص مختلفی دارد که به عنوان بهترین ماده، برای ساخت پروتزهای سیلیکونی شناخته شده است؛ برای مثال، در مقایسه با دیگر موادی که در ساخت پروتزها استفاده میشود، بیشترین اصطکاک را با پوست دارد [6]. این خاصیت، سبب میشود حین استفاده از پروتزهای پارشیال پا که از جنس سیلیکون ساخته شدهاند، پروتز کمترین حرکت را نسبت به پوست داشته باشد. ویژگی بارز دیگری که میتوان برای سیلیکون در نظر گرفت آن است که برخلاف دیگر پلیمرها، که ریشهای نفتی دارند، این ماده، ریشه معدنی دارد (سنگ سیلیکات) و در اثر اختلاف دما، نرم و سخت نمیشود. یعنی دما و دیگر شرایط محیطی، در مقایسه با دیگر مواد، کمترین تغییر را در خواص مکانیکی این پلیمر ایجاد میکند [7].
این ماده در اشکال متنوعی تولید میشود و میتواند در حالت سفت یا برعکس بسیار نرم ساخته شود. زمانی که سیلیکون بسیار نرم تولید میشود، نهتنها پدینگ و نَرمسازی بسیار خوبی ایجاد میکند، بلکه از پوست در برابر سایش و برش نیز محافظت میکند. این نکته میتواند اهمیت زیادی داشته باشد، چون سائیدگی به نوعی مهمترین عامل تخریب پوست و بروز مشکلات پوستی به شمار میآید. در کشورهای صنعتی سازنده ماده اولیه سیلیکون، این ماده با خواص گوناگون و برای مصارف مختلف، تهیه و عرضه میشود و برای ساخت پروتز، نوع Medical grade (که در سختیهای مختلف موجود است) استفاده میشود. بررسی پروتزهای سیلیکونی استفادهشده در این زمینه نشان میدهد پروتزیستها در تمامی موارد از مواد با سختی یکسان در تمام دیوارههای سوکت استفاده میکنند [10-8].
بررسی مطالعات انجامشده در این زمینه نیز نشان داد افزایش درخور توجه فشار در استامپ، بعد از قطع عضو پارشیال پا وجود دارد که این افزایش فشار نیاز به توزیع مناسبتر به صورت ویژه در نقاط پرفشار دارد [12 ،11]. از آنجایی که سوکت پروتزهای سیلیکونی در تمام دیواره سختی یکسان دارد، بالطبع نمیتواند این مشکل را مرتفع کند، بنابراین هدف از انجام این مطالعه در گام نخست، شناسایی نقاط پُرفشار در استامپ حین استفاده از پروتزهای سیلیکونی رایج و در گام دوم استفاده از مواد سیلیکونی با سختی کمتر در نقاط پرفشار و طراحی پروتزی جدید است که باعث توزیع مناسبتر فشار در این افراد شود. به طور کلی هدف ما در این مطالعه طراحی و ساخت پروتز سیلیکونی جدید به منظور کاهش فشارهای موضعی با درنظرگرفتن شرایط استامپ و انتخاب سختیهای مناسب سیلیکون برای این بیماران و درنهایت ارزیابی و مقایسه آن با پروتزهای سیلیکونی مرسوم بود.
روش بررسی
این پژوهش شبهتجربی روی پنج بیمار دیابتی با قطع عضو ترنس متاتارسال (سه زن و دو مرد) در سال 1396 انجام گرفت. نمونهگیری به صورت غیراحتمالی ساده بود و شرکتکنندگان در آزمایشگاه راهرفتن گروه ارتز و پروتز دانشگاه علوم بهزیستی و توانبخشی ارزیابی شدند. ملاکهای ورود به پژوهش عبارت بودند از دیابت نوع ۲، قطع عضو پارشیال پا در سطح ترنسمتاتارسال حداقل در یک اندام که بیش از یک سال از آن گذشته باشد، استفاده از پروتزهای سیلیکونی مرسوم در گذشته حداقل به مدت 3 ماه، توانایی در راهرفتن بدون کمک بیش از 100 متر، نداشتن جراحی اندام تحتانی مانند پروتز هیپ، زانو، مچ و پا، نبود اختلاف طول دو اندام، نداشتن سابقه جراحی یا آسیب به کمر، سن زیر 65 سال، نداشتن زخم در استامپ. ملاکهای خروج از مطالعه نیز ایجاد زخم جدید در استامپ، درد شدید حاصل از نوروما که مانع راهرفتن بیمار شود و تمایلنداشتن بیمار به ادامه همکاری بود [16-13 ،8]. برای جمعآوری اطلاعات از ابزارهایی که در ادامه ذکر شده استفاده شد. دستگاه سنجش فشار کفپایی شرکت ناول آلمان مدل پدار-ایکس برای اندازهگیری فشار کف پایی در طول راهرفتن و شش حسگر سنجش فشار مقاومتی از نوع Force Sensing Resistors (FSR-402, Interlink Electronics) (تصویر شماره ۱). این حسگرها روی نقاطی از استامپ که فشار بیش از ۲۰۰ کیلوپاسکال داشت با چسب ثابت شدند و اطلاعات آنها وارد یک بسته پردازشگر شد که روی ساق قرار گرفته بود.
برای اندازهگیری میزان درد از مقیاس 100 میلیمتری آنالوگ بینایی استفاده شد. از بیماران خواسته شد دردی را که در استامپ خود پس از طی یک کیلومتر راهرفتن احساس میکردند روی نقطهای که به بهترین نحو شدت درد آنها را نشان میداد، علامت بزنند (عدد صفر=بدون درد،20-۱=درد خفیف، 40-۲۱=درد متوسط و اذیتکننده، ۶۰-۴۱=درد نسبتاً شدید، ۸۰-۶۱=درد شدید، ۱۰۰-۸۰=بدترین حالت ممکن) [17]
روش جمعآوری اطلاعات
این مطالعه در سه مرحله انجام گرفت.
مرحله اول
با استفاده از سیستم پدار و در وضعیت بدون پروتز فشارهای کف پایی اندازهگیری شد. برای جمعآوری دادههای مربوط به کفی سنجش فشار پدار و برای شروع آزمون، کفی سنجش فشار داخل کفش آزمون قرار داده شد. برای همه شرکتکنندگان از یک نوع کفش استاندارد استفاده شد. سپس جعبه جمعآوری اطلاعات با کمربند مخصوص دور کمر فرد بسته و سیمهای بین کفی و جعبه جمعآوری اطلاعات با استرپ دور مچ و ران ثابت شد. از هر بیمار خواسته شد مسافت 9متری آزمایشگاه را برای سه دور طی کند و هر بار که به انتهای مسیر میرسد برای سه ثانیه مکث کند و سپس برگردد و به مسیر خود ادامه دهد و در طول تمامی آزمونها با سرعت عادی خود راه برود. زمان طیشده با کورنومتر ثبت شد.
روش جمعآوری اطلاعات
این مطالعه در سه مرحله انجام گرفت.
مرحله اول
با استفاده از سیستم پدار و در وضعیت بدون پروتز فشارهای کف پایی اندازهگیری شد. برای جمعآوری دادههای مربوط به کفی سنجش فشار پدار و برای شروع آزمون، کفی سنجش فشار داخل کفش آزمون قرار داده شد. برای همه شرکتکنندگان از یک نوع کفش استاندارد استفاده شد. سپس جعبه جمعآوری اطلاعات با کمربند مخصوص دور کمر فرد بسته و سیمهای بین کفی و جعبه جمعآوری اطلاعات با استرپ دور مچ و ران ثابت شد. از هر بیمار خواسته شد مسافت 9متری آزمایشگاه را برای سه دور طی کند و هر بار که به انتهای مسیر میرسد برای سه ثانیه مکث کند و سپس برگردد و به مسیر خود ادامه دهد و در طول تمامی آزمونها با سرعت عادی خود راه برود. زمان طیشده با کورنومتر ثبت شد.
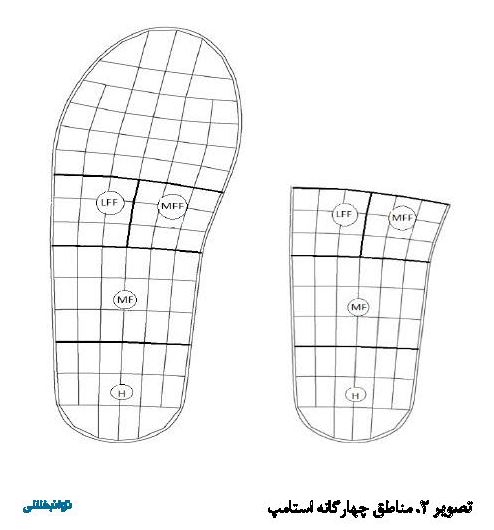
با استفاده از فرمول سرعت برابر است با مسافت طیشده تقسیم بر زمان، سرعت فرد محاسبه شد. این کار ادامه یافت تا زمانی که از هر فرد سه آزمون موفق ثبت شد. برای اندازهگیری فشار کف پایی، پا به چهار منطقه تقسیم شد، شامل پاشنه، قسمت میانی پا و داخل و خارج قسمت جلوی پا (تصویر شماره ۲). میانگین بیشترین فشار هریک از این چهار ناحیه اندازهگیری شد. میزان فشاری که باعث ایجاد زخم میشود در مطالعات مختلف متفاوت است. در مطالعه اوئینگ و همکاران، فشار۲۰۰ کیلوپاسکال به عنوان حد آستانه گزارش شده است [18]. هرچند در مطالعات دیگر این میزان فشار 200 [18]، 600 [19]، ۸۷۵ [20] و 1000 [21] کیلوپاسکال هم اعلام شده است. برای اطمینان خاطر کمترین میزان نیرو یا همان 200 کیلوپاسکال به عنوان حد آستانه در نظر گرفته شد. نقاطی که در آنها حداکثر فشار پلانتار از ۲۰۰ کیلوپاسکال بیشتر بود به عنوان نقاطی با فشارهای موضعی زیاد تعیین شدند [22].
در مرحله بعد، حسگرهای سنجش فشار مقاومتی با لایه نازکی از چسب نواری در نقاط علامتزده ثابت شدند. چهار حسگر در نقاط مشخصشده در مناطق چهارگانه استامپ و 2 حسگر دیگر روی خط بخیه و در سمت داخل و خارج انتهای دیستال استامپ قرار گرفتند (تصویر شماره 3 و ۴). سپس پروتز سیلیکونی مرسوم و کفش آزمون پوشیده شد. هنگامی که بیمار احساس کرد برای شروع آزمون آمادگی لازم را دارد از او خواسته شد تا مسیر 9متری آزمایشگاه را طی کند و به انتهای مسیر که رسید ۳ ثانیه توقف کند و سپس برگردد. با استفاده از کورنومتر زمان طیشده در هر مسیر اندازهگیری شد این کار ادامه یافت تا زمانی که سه آزمون موفق به دست آمد. بین انجام هر آزمون به بیمار چند دقیقه فرصت داده شد تا استراحت کند. درد استامپ هنگام راهرفتن با پروتز سیلیکونی مرسوم با استفاده از مقیاس آنالوگ بینایی اندازهگیری شد.
برای اندازهگیری مدتزمان فازهای استانس و سوئینگ با استفاده از حسگرهای سنجش فشار مقاومتی، ابتدا لحظه برخورد پاشنه با زمین (هیلاستریک) و بعد لحظه جداشدن پنجه از زمین مشخص شد که به ترتیب نشاندهنده لحظه شروع و پایان گام هستند (فاز استانس). هیلاستریک زمانی است که فشار وارد بر سنسور پاشنه نسبت به میزان اولیه خود در حالت بدون تحمل وزن در خط پایه شروع به افزایش میکند. لحظه جداشدن پنجه از زمین زمانی است که فشار وارد بر سنسور ناحیه فورفوت شروع به کاهش میکند تا به کمترین میزان خود میرسد. از لحظه تماس پاشنه استامپ با زمین تا زمانی که استامپ کاملاً از زمین جدا میشود، به عنوان فاز استانس و فاصله زمانی بین جداشدن استامپ از زمین تا تماس دوباره استامپ با زمین به عنوان فاز سوئینگ در نظر گرفته شد.
در مرحله بعد، حسگرهای سنجش فشار مقاومتی با لایه نازکی از چسب نواری در نقاط علامتزده ثابت شدند. چهار حسگر در نقاط مشخصشده در مناطق چهارگانه استامپ و 2 حسگر دیگر روی خط بخیه و در سمت داخل و خارج انتهای دیستال استامپ قرار گرفتند (تصویر شماره 3 و ۴). سپس پروتز سیلیکونی مرسوم و کفش آزمون پوشیده شد. هنگامی که بیمار احساس کرد برای شروع آزمون آمادگی لازم را دارد از او خواسته شد تا مسیر 9متری آزمایشگاه را طی کند و به انتهای مسیر که رسید ۳ ثانیه توقف کند و سپس برگردد. با استفاده از کورنومتر زمان طیشده در هر مسیر اندازهگیری شد این کار ادامه یافت تا زمانی که سه آزمون موفق به دست آمد. بین انجام هر آزمون به بیمار چند دقیقه فرصت داده شد تا استراحت کند. درد استامپ هنگام راهرفتن با پروتز سیلیکونی مرسوم با استفاده از مقیاس آنالوگ بینایی اندازهگیری شد.
برای اندازهگیری مدتزمان فازهای استانس و سوئینگ با استفاده از حسگرهای سنجش فشار مقاومتی، ابتدا لحظه برخورد پاشنه با زمین (هیلاستریک) و بعد لحظه جداشدن پنجه از زمین مشخص شد که به ترتیب نشاندهنده لحظه شروع و پایان گام هستند (فاز استانس). هیلاستریک زمانی است که فشار وارد بر سنسور پاشنه نسبت به میزان اولیه خود در حالت بدون تحمل وزن در خط پایه شروع به افزایش میکند. لحظه جداشدن پنجه از زمین زمانی است که فشار وارد بر سنسور ناحیه فورفوت شروع به کاهش میکند تا به کمترین میزان خود میرسد. از لحظه تماس پاشنه استامپ با زمین تا زمانی که استامپ کاملاً از زمین جدا میشود، به عنوان فاز استانس و فاصله زمانی بین جداشدن استامپ از زمین تا تماس دوباره استامپ با زمین به عنوان فاز سوئینگ در نظر گرفته شد.
مرحله دوم
پروتز سیلیکونی مرسوم که شرکتکنندگان در مطالعه استفاده کرده بودند در همه قسمتها از سیلیکون سخت RTV3040 با سختی ۳۶ (شیمی افسون، تهران) ساخته شده بود. برای ساخت این پروتز با استفاده از آلژینات از استامپ بیمار و همچنین پای مقابل او قالب منفی تهیه و داخل آن با گچ پر میشود. قسمتهای ازدسترفته اندام با استفاده از موم بازسازی و با تزریق سیلیکون، پروتز ساخته میشود. تریملاین این پروتز تا یک سانتیمتر بالای قوزکها بود و در ساخت آن هیچگونه تقویتکننده اضافی به کار نرفته بود. این پروتز را کارشناسی ماهر که تجربه کافی داشت، ساخته بود و اندازهبودن پروتز (از نظر تنگ و گشادبودن) در زمان ساخت و همچنین قبل از آغاز مطالعه را بررسی و تأیید کرده بود.
برای ساخت پروتز سیلیکونی جدید از دو نوع سیلیکون با سختیهای مختلف استفاده شد؛ سیلیکون RTV4407 با سختی ۷ محصول شرکت بلاستر فرانسه، در نقاط پرفشار و سیلیکون RTV3040 با سختی ۳۶ در دیوارهها. تریملاین این پروتز مانند پروتز سیلیکونی مرسوم بود و در ساخت آن از هیچ نوع تقویتکنندهای استفاده نشده بود [23]. کارشناس ماهر و با تجربه که قبلاً پروتز سیلیکونی مرسوم را ساخته بود، این پروتز را قالبگیری کرد و ساخت تا از نظر اندازه پروتز و حدود دیوارهها با پروتز مرسوم یکسان باشد.
مرحله سوم
از هریک از شرکتکنندگان خواسته شد تا پروتز را 3 هفته بپوشند تا به آن عادت کنند [8] و پس از پایان این مدت برای ارزیابی مجدد، دوباره مراجعه کنند. در ابتدای شروع آزمون، حسگرهای سنجش فشار مقاومتی در نقاطی از استامپ که فشار پلانتار بیش از ۲۰۰ کیلوپاسکال داشتند با چسب نصب شدند و اطلاعات فشار با این حسگرها اندازهگیری شد. این نقاط در فاز اول مطالعه مشخص شده بودند و پروتز سیلیکونی جدید که برای هر بیمار به صورت مجزا ساخته شد، در این نقاط سیلیکون نرم داشت.
بیمار مسیر 9متری طول آزمایشگاه را با سرعت عادی راهرفتن، سه بار طی کرد و در هر بار با استفاده از کورنومتر زمان طیشده ثبت شد. بدین ترتیب سرعت راهرفتن در هر بار محاسبه شد و میانگین آنها به عنوان سرعت بیمار در نظر گرفته شد. طبق همان شرایطی که پیشتر در فاز اول مطالعه توضیح داده شد پارامترهای مربوط به راهرفتن و درد اندازهگیری شدند.
برای بررسی عادیبودن توزیع دادهها از آزمون شاپیروویلکز و از آزمونهای میانگین، انحراف معیار و میزان خطای استاندارد برای توصیف دادهها استفاده شد. دادهها با استفاده از نسخه 17 نرمافزار آماری SPSS و آزمون تیزوجی در سطح معنیداری کمتر از ۵ درصد تجزیه و تحلیل شدند.
پروتز سیلیکونی مرسوم که شرکتکنندگان در مطالعه استفاده کرده بودند در همه قسمتها از سیلیکون سخت RTV3040 با سختی ۳۶ (شیمی افسون، تهران) ساخته شده بود. برای ساخت این پروتز با استفاده از آلژینات از استامپ بیمار و همچنین پای مقابل او قالب منفی تهیه و داخل آن با گچ پر میشود. قسمتهای ازدسترفته اندام با استفاده از موم بازسازی و با تزریق سیلیکون، پروتز ساخته میشود. تریملاین این پروتز تا یک سانتیمتر بالای قوزکها بود و در ساخت آن هیچگونه تقویتکننده اضافی به کار نرفته بود. این پروتز را کارشناسی ماهر که تجربه کافی داشت، ساخته بود و اندازهبودن پروتز (از نظر تنگ و گشادبودن) در زمان ساخت و همچنین قبل از آغاز مطالعه را بررسی و تأیید کرده بود.
برای ساخت پروتز سیلیکونی جدید از دو نوع سیلیکون با سختیهای مختلف استفاده شد؛ سیلیکون RTV4407 با سختی ۷ محصول شرکت بلاستر فرانسه، در نقاط پرفشار و سیلیکون RTV3040 با سختی ۳۶ در دیوارهها. تریملاین این پروتز مانند پروتز سیلیکونی مرسوم بود و در ساخت آن از هیچ نوع تقویتکنندهای استفاده نشده بود [23]. کارشناس ماهر و با تجربه که قبلاً پروتز سیلیکونی مرسوم را ساخته بود، این پروتز را قالبگیری کرد و ساخت تا از نظر اندازه پروتز و حدود دیوارهها با پروتز مرسوم یکسان باشد.
مرحله سوم
از هریک از شرکتکنندگان خواسته شد تا پروتز را 3 هفته بپوشند تا به آن عادت کنند [8] و پس از پایان این مدت برای ارزیابی مجدد، دوباره مراجعه کنند. در ابتدای شروع آزمون، حسگرهای سنجش فشار مقاومتی در نقاطی از استامپ که فشار پلانتار بیش از ۲۰۰ کیلوپاسکال داشتند با چسب نصب شدند و اطلاعات فشار با این حسگرها اندازهگیری شد. این نقاط در فاز اول مطالعه مشخص شده بودند و پروتز سیلیکونی جدید که برای هر بیمار به صورت مجزا ساخته شد، در این نقاط سیلیکون نرم داشت.
بیمار مسیر 9متری طول آزمایشگاه را با سرعت عادی راهرفتن، سه بار طی کرد و در هر بار با استفاده از کورنومتر زمان طیشده ثبت شد. بدین ترتیب سرعت راهرفتن در هر بار محاسبه شد و میانگین آنها به عنوان سرعت بیمار در نظر گرفته شد. طبق همان شرایطی که پیشتر در فاز اول مطالعه توضیح داده شد پارامترهای مربوط به راهرفتن و درد اندازهگیری شدند.
برای بررسی عادیبودن توزیع دادهها از آزمون شاپیروویلکز و از آزمونهای میانگین، انحراف معیار و میزان خطای استاندارد برای توصیف دادهها استفاده شد. دادهها با استفاده از نسخه 17 نرمافزار آماری SPSS و آزمون تیزوجی در سطح معنیداری کمتر از ۵ درصد تجزیه و تحلیل شدند.
یافتهها
در این مطالعه پنج بیمار مبتلا به دیابت نوع 2 شرکت داشتند. این افراد همگی دچار قطع عضو از سطح ترنسمتاتارسال بودند و پزشک متخصص غدد یا ارتوپد آنها را ارجاع داده بود. تمامی شرکتکنندگان قبلاً از پروتز سیلیکونی مرسوم، حداقل سه ماه استفاده کرده بودند، ولی از درد و سوزش در استامپ حین راهرفتن با پروتز شکایت داشتند (جدول شماره ۱).
فشار کف پایی با استفاده از حسگرهای سنجش فشار مقاومتی در شش نقطه از استامپ برای هر شرکتکننده به طور مجزا اندازهگیری شد. برای بررسی عادیبودن توزیع دادهها از آزمون شاپیروویلکز استفاده شد. میانگین و انحراف معیار فشار کف پایی در هر نقطه برای افراد آمپوته در دو حالت با پروتز سیلیکونی مرسوم و پروتز سیلیکونی جدید در جدول شماره ۲ نمایش داده شده است. همانطور که در جدول شماره ۲ نشان داده شده است تمامی متغیرها توزیع عادی دارند، درنتیجه برای مقایسه تأثیر دو پروتز از آزمون تی زوج استفاده شد.
در این مطالعه پنج بیمار مبتلا به دیابت نوع 2 شرکت داشتند. این افراد همگی دچار قطع عضو از سطح ترنسمتاتارسال بودند و پزشک متخصص غدد یا ارتوپد آنها را ارجاع داده بود. تمامی شرکتکنندگان قبلاً از پروتز سیلیکونی مرسوم، حداقل سه ماه استفاده کرده بودند، ولی از درد و سوزش در استامپ حین راهرفتن با پروتز شکایت داشتند (جدول شماره ۱).
فشار کف پایی با استفاده از حسگرهای سنجش فشار مقاومتی در شش نقطه از استامپ برای هر شرکتکننده به طور مجزا اندازهگیری شد. برای بررسی عادیبودن توزیع دادهها از آزمون شاپیروویلکز استفاده شد. میانگین و انحراف معیار فشار کف پایی در هر نقطه برای افراد آمپوته در دو حالت با پروتز سیلیکونی مرسوم و پروتز سیلیکونی جدید در جدول شماره ۲ نمایش داده شده است. همانطور که در جدول شماره ۲ نشان داده شده است تمامی متغیرها توزیع عادی دارند، درنتیجه برای مقایسه تأثیر دو پروتز از آزمون تی زوج استفاده شد.
بر اساس جدول شماره ۲ مشاهده میشود هنگام راهرفتن با پروتز سیلیکونی مرسوم، بیشترین فشار در ناحیه جلوی استامپ و سمت خارج خط بخیه وجود دارد. در حالی که این میزان فشار هنگام راهرفتن با پروتز سیلیکونی جدید به میزان زیادی کاهش یافته است و به زیر حد آستانه رسیده است. به بیان دیگر افراد آمپوته پارشیال پا هنگام راهرفتن با پروتز سیلیکونی جدید فشار موضعی کمتری متحمل میشدند.
از تصویر شماره 5 برای درک بهتر تأثیر پروتز سیلیکونی جدید بر فشارهای کف پایی در نقاط ششگانه استامپ استفاده شده است و مشاهده میشود میزان فشار در ناحیه پاشنه در همه نمونهها روند کاهشی داشته است. این میزان کاهش به طور متوسط برابر 61 درصد میزان اولیه در همه شرکتکنندگان بوده است. در جدول شماره 2 مشخص میشود میانگین حداکثر فشار در قسمت میانی استامپ بین پنج شرکتکننده هنگام استفاده از پروتز سیلیکونی مرسوم 36±267 بوده است. این میزان پس از استفاده از پروتز سیلیکونی جدید به 22±159 کیلوپاسکال رسیده است.
از تصویر شماره 5 برای درک بهتر تأثیر پروتز سیلیکونی جدید بر فشارهای کف پایی در نقاط ششگانه استامپ استفاده شده است و مشاهده میشود میزان فشار در ناحیه پاشنه در همه نمونهها روند کاهشی داشته است. این میزان کاهش به طور متوسط برابر 61 درصد میزان اولیه در همه شرکتکنندگان بوده است. در جدول شماره 2 مشخص میشود میانگین حداکثر فشار در قسمت میانی استامپ بین پنج شرکتکننده هنگام استفاده از پروتز سیلیکونی مرسوم 36±267 بوده است. این میزان پس از استفاده از پروتز سیلیکونی جدید به 22±159 کیلوپاسکال رسیده است.
فشار کف پایی در سمت خارج ناحیه جلوی استامپ نسبت به سمت داخل، ناحیه میانی استامپ و پاشنه در آمپوته اول و دوم هنگام راهرفتن با پروتز سیلیکونی موسوم بیشتر بوده است. هنگام استفاده از پروتز سیلیکونی مرسوم، حداکثر فشار در سمت خارج و جلوی استامپ برابر ۴۴۰ کیلوپاسکال و مربوط به شرکتکننده اول و حداقل فشار ۲۳1 کیلوپاسکال مربوط به شرکتکننده پنجم بود. میانگین فشار در سمت خارج فورفوت در همه شرکتکنندگان 9۰±299 کیلوپاسکال بود. پس از استفاده از پروتز سیلیکونی جدید، حداکثر فشار جلوی استامپ، در سمت خارج ۱۹۱ و در سمت داخل ۱89 کیلوپاسکال و مربوط به شرکتکننده اول بود. با توجه به تصویر شماره 6، هنگام راهرفتن با پروتز سیلیکونی مرسوم آمپوتههای 1، 3 و 5 درد نسبتاً شدید و آمپوتههای 2 و 4 درد متوسط ولی اذیتکنندهای را احساس میکردند. ولی هنگام راهرفتن با پروتز سیلیکونی جدید به دنبال کاهش فشارهای موضعی، درد در آمپوتهها کاهش یافت و همگی درد خفیف داشتند.
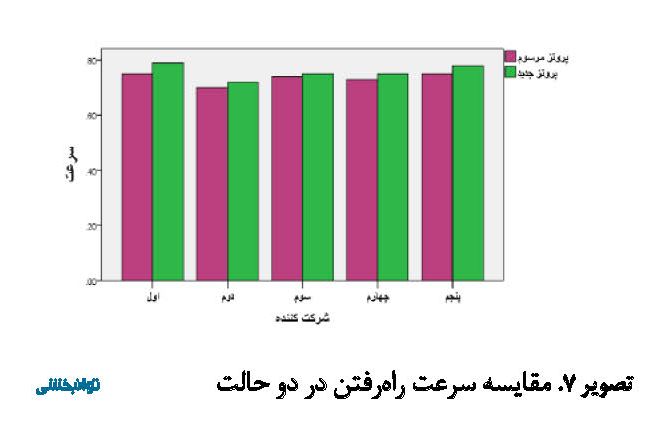
در تصویر شماره 7 مشخص شده است سرعت راهرفتن نمونهها با پروتز سیلیکونی جدید، با شیب ملایمی افزایش یافته به جز در آمپوته سه که میزان افزایش سرعت کمتر از دیگر نمونهها بوده است. به صورت کلی با مقایسه میانگینها میتوان عنوان کرد سرعت راهرفتن افراد آمپوته حین استفاده از پروتز جدید نسبت به پروتز مرسوم به میزان اندکی افزایش داشته است.
در تصویر شماره 7 مشخص شده است سرعت راهرفتن نمونهها با پروتز سیلیکونی جدید، با شیب ملایمی افزایش یافته به جز در آمپوته سه که میزان افزایش سرعت کمتر از دیگر نمونهها بوده است. به صورت کلی با مقایسه میانگینها میتوان عنوان کرد سرعت راهرفتن افراد آمپوته حین استفاده از پروتز جدید نسبت به پروتز مرسوم به میزان اندکی افزایش داشته است.
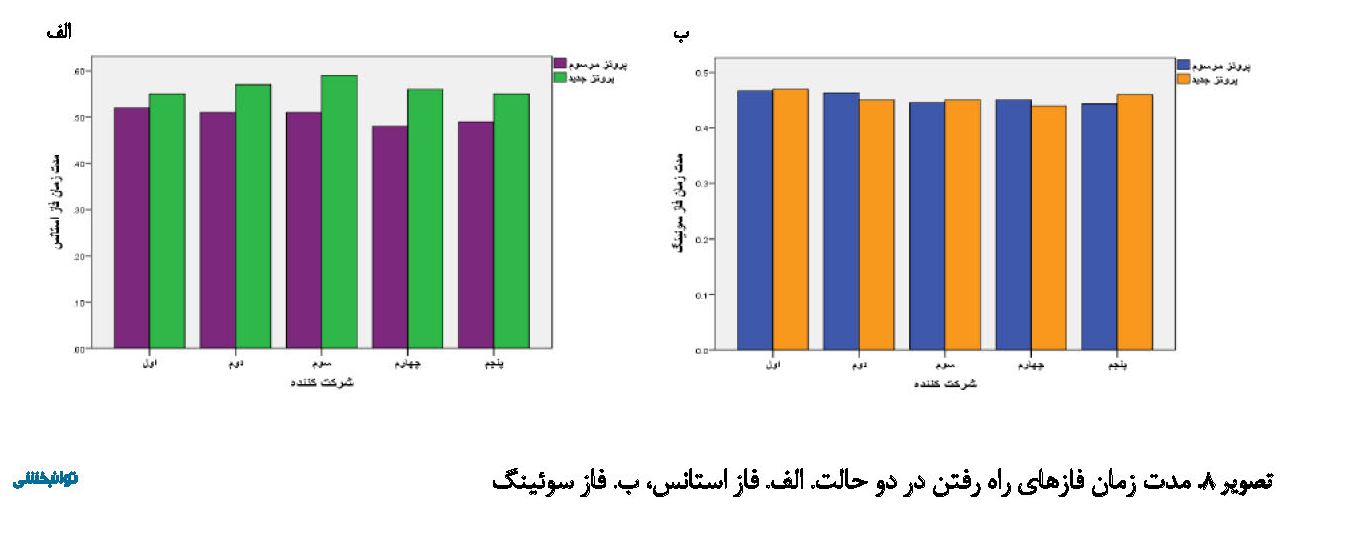
در مقایسه مدتزمان فاز استانس و سوئینگ افراد آمپوته نیز از نمودار خطی استفاده شده است. همانطور که در تصویر شماره 8 مشاهده میشود آمپوته 4 کمترین زمان فاز استانس را حین استفاده از پروتز مرسوم داشته است. هنگام استفاده از پروتز سیلیکونی جدید مدتزمان فاز استانس در همه نمونهها افزایش داشته است، ولی آمپوته 3 بیشترین میزان افزایش را تجربه کرده است.
بحث
پروتز طراحیشده در مطالعه حاضر با داشتن ساختار و سازوکارهای لازم توانسته است سبب کاهش درد در استامپ حین راهرفتن شود. با استفاده از پروتز سیلیکونی جدید، میانگین حداکثر فشار کف پایی در قسمت داخل و خارج ناحیه جلوی استامپ، خط بخیه، قسمت میانی استامپ و پاشنه کاهش یافت. همچنین مدتزمان فاز استانس و سرعت راهرفتن افزایش داشت، ولی تغییری در مدتزمان فاز سوئینگ مشاهده نشد.
بحث
پروتز طراحیشده در مطالعه حاضر با داشتن ساختار و سازوکارهای لازم توانسته است سبب کاهش درد در استامپ حین راهرفتن شود. با استفاده از پروتز سیلیکونی جدید، میانگین حداکثر فشار کف پایی در قسمت داخل و خارج ناحیه جلوی استامپ، خط بخیه، قسمت میانی استامپ و پاشنه کاهش یافت. همچنین مدتزمان فاز استانس و سرعت راهرفتن افزایش داشت، ولی تغییری در مدتزمان فاز سوئینگ مشاهده نشد.
مطالعه منتشرشدهای که تأثیر سیلیکون را بر توزیع فشار کف پایی در افراد آمپوته پارشیال پا بررسی کند، یافت نشد، اما بررسی مطالعات انجامشده در زمینه تأثیر کفیهای سیلیکونی بر کاهش فشار در افراد دیابتی نشان میدهد در کفی بیماران دیابتی به علت نقص حسی، لایهای که در تماس با پاست از مواد نرمتر انتخاب میشود تا فشار وارد به کف پا را کاهش دهد [24]. مطالعات گذشته نشان داده است کفی طبی بیماران دیابتی باید با ترکیبی از چند ماده ساخته شود، زیرا هر ماده خصوصیات فیزیکی و مکانیکی (دانسیته، سفتی، قابلیت فشردگی و دوام) مخصوص به خود دارد و ترکیب چند ماده در ساختار کفی طبی سبب تقویت خصوصیات مثبت مواد و کاهش نقاط ضعف آنها میشود [26 ،25].
در مطالعه حاضر از سیلیکون نرم RTV 4407 A/B به ضخامت 3 میلیمتر و با شور ۷ در لایه داخلی پروتز (در مناطق پرفشار و در معرض خطر زخمشدن) و سیلیکون سفت RTV 3040 با شور ۳۶ به ضخامت 5 میلیمتر در لایه زیرین و خارجی و دیوارههای پروتز استفاده شده است.
نتایج مطالعه حاضر نشان داد پروتز سیلیکونی جدید سبب تغییر میانگین حداکثر فشار در تمامی مناطق ششگانه استامپ میشود. استفاده از پروتز سیلیکونی جدید سبب کاهش فشار در ناحیه پاشنه، قسمت میانی پا، سمت داخل و خارج قسمت جلوی استامپ و سمت داخل و خارج خط بخیه شده است. با وجود اینکه توزیع فشار در تمامی نواحی پا با استفاده از پروتز سیلیکونی جدید نسبت به پروتز سیلیکونی مرسوم تغییر کرده، ولی این تغییر در ناحیه جلوی استامپ خصوصاً سمت خارج بیشتر بوده است.
کاهش فشار موضعی در کف پا باعث انتقال فشار به دیگر نقاط میشود. بنابراین فشار در کل سطح کف پا توزیع میشود. با آمپوتاسیون پارشیال پا تنشن عضلات ناحیه داخل مچ کاهش مییابد و به علت قطع اینسرشن عضلات دورسی فلکسور و کشش عضلات تریسپس سورآ، استامپ بیمار به اکواینوس و به دنبال آن واروس متمایل میشود. به علت اکواینوواروس و کاهش قدرت عضلات اورتور، فشار پلانتار بیشتر به سمت خارج استامپ انتقال مییابد [27].
در مطالعه ما، نتایج استفاده از پروتز سیلیکونی جدید پس از 3 هفته نشان داد فشار کف پایی در ناحیه جلوی پا کاهش چشمگیری داشته است؛ به طوری که در تمامی نمونهها میانگین حداکثر فشار به زیر حد آستانه رسید. این امر نشان میدهد سیلیکون نرم استفادهشده در پروتز جدید میتواند نرمی و راحتی موردنیاز را در آمپوتههای دیابتی مطالعهشده فراهم کند. به همین دلیل آمپوتههای مطالعهشده حین راهرفتن با پروتز سیلیکونی جدید نسبت به پروتز سیلیکونی مرسوم درد کمتری احساس میکردند و قادر بودند با سرعت بیشتری راه بروند.
مطالعه دیلون و همکاران در سال 2006 نشان دادند افراد قطع عضو پارشیال پا به علت ترس از اعمال فشار روی نقاط مستعد آسیب نمیتوانند با این نوع پروتزها با سرعت حداکثری راه بروند. بنابراین این افراد در حین راهرفتن با پروتزهای پارشیال پا سرعتشان افزایش نمییابد.
البته گاهیاوقات ترس از اعمال فشار در نقاط قدامی سطح پلانتار پا در پروتزهایی که از دیوارهها تا قوزکها امتداد دارند میتواند باعث شود فرد با سرعتهای بیشتر راه نرود [28]. این یافته نشان میدهد الگوی راهرفتن در بیماران دیابتی، الگویی محتاطانه است؛ به صورتی که این بیماران برای جلوگیری از اعمال فشار بیش از حد به ناحیه پلانتار پا سرعت راهرفتن را کاهش میدهند و به نحو بارزی آهستهتر از افراد غیردیابتی در همین گروه سنی راه میروند و این کاهش سرعت با کاهش تعداد گامها و افزایش مدتزمان سیکل راهرفتن اتفاق میافتد [30 ،29].
نتایج مطالعه حاضر نشان میدهد مدتزمان انجام هر گام در شرکتکنندگان در مطالعه افزایش یافته است به این صورت که زمان استانس افزایش یافته است، ولی مدتزمان فاز سوئینگ تقریباً تغییری نداشته است. این امر نشاندهنده افزایش فاز سوئینگ در پای مقابل است. به بیان دیگر استفاده از پروتز سیلیکونی جدید باعث شده است افراد آمپوته به علت کاهش درد، با اطمینان بیشتری روی پای آمپوتهشده تحمل وزن کنند و این امر باعث میشود هنگام راهرفتن نیروی کمتری به پای مقابل اعمال شود.
نتیجهگیری
پروتز سیلیکونی جدید ساختهشده در مطالعه حاضر با داشتن سختیهای متفاوت سیلیکون توانسته است به میزان زیادی از فشارهای نقطهای بکاهد و فشار حاصل از تحمل وزن را بر کل سطح پلانتار باقیمانده اندام به صورت یکنواخت توزیع کند. ایجاد اطمینان به پروتز باعث شده است افراد شرکتکننده در این مطالعه، احساس رضایت بیشتری هنگام استفاده از آن داشته باشند و تمایل بیشتری به راهرفتن از خود نشان دهند.
مقایسه پروتز مرسوم که مدت استفاده از آن به طور متوسط یک سال بود با پروتز جدید که بیماران به مدت 3 هفته از آن استفاده کرده بودند، یکی از محدودیتهای تحقیق بود که اگر مدتزمان استفاده برابر بود، شاید نتایج بهتری حاصل میشد. به علاوه، در کشور ما به علت محدودیت در پوشش بیمهای یا هر نوع حمایت مالی از آمپوتهها برای تأمین هزینه مالی ساخت پروتز، بسیاری از آمپوتهها امکان استفاده از پروتز را ندارند.
در مطالعه حاضر از آنجایی که افراد مطالعهشده باید در گذشته از پروتز سیلیکونی مرسوم استفاده میکردند، پیداکردن تعداد بیشتر این افراد برای گروه کنترل به صورت جداگانه امکانپذیر نبود و بهناچار مطالعه به صورت قبلبعد طراحی شد. از طرف دیگر تعداد مقالات چاپشده در دنیا درباره پروتزهای سیلیکونی پارشیال پا اندک است و امکان ارزیابی و بحثهای عمیق درباره چگونگی عملکرد و مکانیسمهای این پروتزها در حال حاضر نبود.
محققان این مطالعه، انجام مطالعهای مشابه با پروتز سیلیکونی جدید و بررسی نیروها و فشارهای وارده به هر دو پای بیماران با استفاده از دستگاه آنالیز راهرفتن و همچنین بررسی میزان رضایتمندی بیماران از پروتز سیلیکونی جدید و مقایسه آن با پروتز سیلیکونی مرسوم را پیشنهاد میکنند.
ملاحظات اخلاقی
پیروی از اصول اخلاق پژوهش
این طرح در کمیته اخلاق دانشگاه علوم بهزیستی و توانبخشی با کد IR.USWR.REC.1394.383 به تصویب رسید. تمام موارد زیر حین تحقیق انجام شد: 1. از تمام بیماران موافقت آگاهانه و کتبی اخذ شد؛ 2. تمامی شرایط آزمون برای بیماران توضیح داده شد؛ 3. هزینه پروتز و آزمونها از شرکتکنندگان گرفته نشد و محقق متعهد به جبران هرگونه هزینه احتمالی تحمیلی ناشی از شرکت در این مطالعه به افراد مورد مطالعه شد؛ 4. هر زمان که آزمونشوندهها احساس خستگی کردند آزمون متوقف شده و شرکتکنندهها مختار بودند در هر مرحله از تحقیق به هر علتی و یا حتی بدون هیچ علتی از ادامه همکاری انصراف دهند؛ 5. اطلاعات جمعآوری شده از افراد شرکتکننده محافظت و اصل رازداری رعایت شد؛ 6. محقق متعهد شد در استفاده، ارائه و نشر مطالب علمی امانتدار باشد و تمامی حقوق محققین را لحاظ کند؛ 7. محقق متعهد شد تمامی نکات و تذکرات اخلاقی را که کمیته اخلاق دانشگاه مطرح و رسماً ابلاغ نموده است در مورد این طرح رعایت کند؛ 8. محقق خود را متعهد به جبران هرگونه هزینه احتمالی تحمیلی ناشی از شرکت در این مطالعه به افراد مورد مطالعه میداند.
حامی مالی
این مقاله برگرفته از پایاننامه دکترای نویسنده اول خانم دکتر فاطمه زارعزاده، گروه ارتز و پروتز دانشگاه علوم بهزیستی و توانبخشی است.
مشارکت نویسندگان
مفهومسازی: محمدعلی مردانی؛ روششناسی: محمدعلی مردانی، محمود بهرامیزاده، فاطمه زارعزاده؛ تحقیق و بررسی: فاطمه زارعزاده، مختار عراضپور، محمدعلی مردانی؛ ویراستاری و نهاییسازی نوشته: فاطمه زارعزاده.
تعارض منافع
بنابر اظهار نویسندگان، این مقاله تعارض منافع ندارد.
در مطالعه حاضر از سیلیکون نرم RTV 4407 A/B به ضخامت 3 میلیمتر و با شور ۷ در لایه داخلی پروتز (در مناطق پرفشار و در معرض خطر زخمشدن) و سیلیکون سفت RTV 3040 با شور ۳۶ به ضخامت 5 میلیمتر در لایه زیرین و خارجی و دیوارههای پروتز استفاده شده است.
نتایج مطالعه حاضر نشان داد پروتز سیلیکونی جدید سبب تغییر میانگین حداکثر فشار در تمامی مناطق ششگانه استامپ میشود. استفاده از پروتز سیلیکونی جدید سبب کاهش فشار در ناحیه پاشنه، قسمت میانی پا، سمت داخل و خارج قسمت جلوی استامپ و سمت داخل و خارج خط بخیه شده است. با وجود اینکه توزیع فشار در تمامی نواحی پا با استفاده از پروتز سیلیکونی جدید نسبت به پروتز سیلیکونی مرسوم تغییر کرده، ولی این تغییر در ناحیه جلوی استامپ خصوصاً سمت خارج بیشتر بوده است.
کاهش فشار موضعی در کف پا باعث انتقال فشار به دیگر نقاط میشود. بنابراین فشار در کل سطح کف پا توزیع میشود. با آمپوتاسیون پارشیال پا تنشن عضلات ناحیه داخل مچ کاهش مییابد و به علت قطع اینسرشن عضلات دورسی فلکسور و کشش عضلات تریسپس سورآ، استامپ بیمار به اکواینوس و به دنبال آن واروس متمایل میشود. به علت اکواینوواروس و کاهش قدرت عضلات اورتور، فشار پلانتار بیشتر به سمت خارج استامپ انتقال مییابد [27].
در مطالعه ما، نتایج استفاده از پروتز سیلیکونی جدید پس از 3 هفته نشان داد فشار کف پایی در ناحیه جلوی پا کاهش چشمگیری داشته است؛ به طوری که در تمامی نمونهها میانگین حداکثر فشار به زیر حد آستانه رسید. این امر نشان میدهد سیلیکون نرم استفادهشده در پروتز جدید میتواند نرمی و راحتی موردنیاز را در آمپوتههای دیابتی مطالعهشده فراهم کند. به همین دلیل آمپوتههای مطالعهشده حین راهرفتن با پروتز سیلیکونی جدید نسبت به پروتز سیلیکونی مرسوم درد کمتری احساس میکردند و قادر بودند با سرعت بیشتری راه بروند.
مطالعه دیلون و همکاران در سال 2006 نشان دادند افراد قطع عضو پارشیال پا به علت ترس از اعمال فشار روی نقاط مستعد آسیب نمیتوانند با این نوع پروتزها با سرعت حداکثری راه بروند. بنابراین این افراد در حین راهرفتن با پروتزهای پارشیال پا سرعتشان افزایش نمییابد.
البته گاهیاوقات ترس از اعمال فشار در نقاط قدامی سطح پلانتار پا در پروتزهایی که از دیوارهها تا قوزکها امتداد دارند میتواند باعث شود فرد با سرعتهای بیشتر راه نرود [28]. این یافته نشان میدهد الگوی راهرفتن در بیماران دیابتی، الگویی محتاطانه است؛ به صورتی که این بیماران برای جلوگیری از اعمال فشار بیش از حد به ناحیه پلانتار پا سرعت راهرفتن را کاهش میدهند و به نحو بارزی آهستهتر از افراد غیردیابتی در همین گروه سنی راه میروند و این کاهش سرعت با کاهش تعداد گامها و افزایش مدتزمان سیکل راهرفتن اتفاق میافتد [30 ،29].
نتایج مطالعه حاضر نشان میدهد مدتزمان انجام هر گام در شرکتکنندگان در مطالعه افزایش یافته است به این صورت که زمان استانس افزایش یافته است، ولی مدتزمان فاز سوئینگ تقریباً تغییری نداشته است. این امر نشاندهنده افزایش فاز سوئینگ در پای مقابل است. به بیان دیگر استفاده از پروتز سیلیکونی جدید باعث شده است افراد آمپوته به علت کاهش درد، با اطمینان بیشتری روی پای آمپوتهشده تحمل وزن کنند و این امر باعث میشود هنگام راهرفتن نیروی کمتری به پای مقابل اعمال شود.
نتیجهگیری
پروتز سیلیکونی جدید ساختهشده در مطالعه حاضر با داشتن سختیهای متفاوت سیلیکون توانسته است به میزان زیادی از فشارهای نقطهای بکاهد و فشار حاصل از تحمل وزن را بر کل سطح پلانتار باقیمانده اندام به صورت یکنواخت توزیع کند. ایجاد اطمینان به پروتز باعث شده است افراد شرکتکننده در این مطالعه، احساس رضایت بیشتری هنگام استفاده از آن داشته باشند و تمایل بیشتری به راهرفتن از خود نشان دهند.
مقایسه پروتز مرسوم که مدت استفاده از آن به طور متوسط یک سال بود با پروتز جدید که بیماران به مدت 3 هفته از آن استفاده کرده بودند، یکی از محدودیتهای تحقیق بود که اگر مدتزمان استفاده برابر بود، شاید نتایج بهتری حاصل میشد. به علاوه، در کشور ما به علت محدودیت در پوشش بیمهای یا هر نوع حمایت مالی از آمپوتهها برای تأمین هزینه مالی ساخت پروتز، بسیاری از آمپوتهها امکان استفاده از پروتز را ندارند.
در مطالعه حاضر از آنجایی که افراد مطالعهشده باید در گذشته از پروتز سیلیکونی مرسوم استفاده میکردند، پیداکردن تعداد بیشتر این افراد برای گروه کنترل به صورت جداگانه امکانپذیر نبود و بهناچار مطالعه به صورت قبلبعد طراحی شد. از طرف دیگر تعداد مقالات چاپشده در دنیا درباره پروتزهای سیلیکونی پارشیال پا اندک است و امکان ارزیابی و بحثهای عمیق درباره چگونگی عملکرد و مکانیسمهای این پروتزها در حال حاضر نبود.
محققان این مطالعه، انجام مطالعهای مشابه با پروتز سیلیکونی جدید و بررسی نیروها و فشارهای وارده به هر دو پای بیماران با استفاده از دستگاه آنالیز راهرفتن و همچنین بررسی میزان رضایتمندی بیماران از پروتز سیلیکونی جدید و مقایسه آن با پروتز سیلیکونی مرسوم را پیشنهاد میکنند.
ملاحظات اخلاقی
پیروی از اصول اخلاق پژوهش
این طرح در کمیته اخلاق دانشگاه علوم بهزیستی و توانبخشی با کد IR.USWR.REC.1394.383 به تصویب رسید. تمام موارد زیر حین تحقیق انجام شد: 1. از تمام بیماران موافقت آگاهانه و کتبی اخذ شد؛ 2. تمامی شرایط آزمون برای بیماران توضیح داده شد؛ 3. هزینه پروتز و آزمونها از شرکتکنندگان گرفته نشد و محقق متعهد به جبران هرگونه هزینه احتمالی تحمیلی ناشی از شرکت در این مطالعه به افراد مورد مطالعه شد؛ 4. هر زمان که آزمونشوندهها احساس خستگی کردند آزمون متوقف شده و شرکتکنندهها مختار بودند در هر مرحله از تحقیق به هر علتی و یا حتی بدون هیچ علتی از ادامه همکاری انصراف دهند؛ 5. اطلاعات جمعآوری شده از افراد شرکتکننده محافظت و اصل رازداری رعایت شد؛ 6. محقق متعهد شد در استفاده، ارائه و نشر مطالب علمی امانتدار باشد و تمامی حقوق محققین را لحاظ کند؛ 7. محقق متعهد شد تمامی نکات و تذکرات اخلاقی را که کمیته اخلاق دانشگاه مطرح و رسماً ابلاغ نموده است در مورد این طرح رعایت کند؛ 8. محقق خود را متعهد به جبران هرگونه هزینه احتمالی تحمیلی ناشی از شرکت در این مطالعه به افراد مورد مطالعه میداند.
حامی مالی
این مقاله برگرفته از پایاننامه دکترای نویسنده اول خانم دکتر فاطمه زارعزاده، گروه ارتز و پروتز دانشگاه علوم بهزیستی و توانبخشی است.
مشارکت نویسندگان
مفهومسازی: محمدعلی مردانی؛ روششناسی: محمدعلی مردانی، محمود بهرامیزاده، فاطمه زارعزاده؛ تحقیق و بررسی: فاطمه زارعزاده، مختار عراضپور، محمدعلی مردانی؛ ویراستاری و نهاییسازی نوشته: فاطمه زارعزاده.
تعارض منافع
بنابر اظهار نویسندگان، این مقاله تعارض منافع ندارد.
References
Basu S, Yudkin JS, Kehlenbrink S, Davies JI, Wild SH, Lipska KJ, et al. Estimation of global insulin use for type 2 diabetes, 2018-30: A microsimulation analysis. The Lancet Diabetes & Endocrinology. 2019; 7(1):25-33. [DOI:10.1016/S2213-8587(18)30303-6]
Armstrong D, Lavery L. Clinical care of the diabetic foot. Arlington, Virginia: American Diabetes Association; 2010.
Apelqvist J. The Diabetic Foot Syndrome Today: A Pandemic Uprise. The Diabetic Foot Syndrome. 2018; 26(1):1-18. [DOI:10.1159/000480040]
Sage RA. Biomechanics of ambulation after partial foot amputation: prevention and management of reulceration. Journal of Prosthetics and Orthotics. 2007; 19(8):P77-P9. [DOI:10.1097/JPO.0b013e3180dc92fb]
Stills ML. Partial foot prostheses/orthoses. Clinical Prosthetics & Orthotics. 1987; 12(1):14-8.
Zhang M, Mak A. In vivo friction properties of human skin. Prosthetics and Orthotics International. 1999; 23(2):135-41.
Polyzois GL, Tarantili PA, Frangou MJ, Andreopoulos AG. Physical properties of a silicone prosthetic elastomer stored in simulated skin secretions. The Journal of Prosthetic Dentistry. 2000; 83(5):572-7. [DOI:10.1016/S0022-3913(00)70017-5]
Burger H, Erzar D, Maver T, Olenšek A, Cikajlo I, Matjačić Z. Biomechanics of walking with silicone prosthesis after midtarsal (Chopart) disarticulation. Clinical Biomechanics. 2009; 24(6):510-6. [DOI:10.1016/j.clinbiomech.2009.03.010] [PMID]
Pollard J, Hamilton GA, Rush SM, Ford LA. Mortality and morbidity after transmetatarsal amputation: retrospective review of 101 cases. The Journal of Foot and Ankle Surgery. 2006; 45(2):91-7. [DOI:10.1053/j.jfas.2005.12.011] [PMID]
Lange LR. The lange silicone partial foot prosthesis. Journal of Prosthetics and Orthotics. 1991; 4(1):56-61. [DOI:10.1097/00008526-199100410-00007]
Armstrong D, Lavery L. Plantar pressures are higher in diabetic patients following partial foot amputation. Ostomy/Wound Management. 1998; 44(3):30-2. [PMID]
Garbalosa JC, Cavanagh PR, Wu G, Ulbrecht JS, Becker MB, Alexander IJ, et al. Foot function in diabetic patients after partial amputation. Foot & Ankle International. 1996; 17(1):43-8. [DOI:10.1177/107110079601700110] [PMID]
Robinson CC, Balbinot LF, Silva MF, Achaval M, Zaro MA. Plantar pressure distribution patterns of individuals with prediabetes in comparison with healthy individuals and individuals with diabetes. Journal of Diabetes Science and Technology. 2013; 7(5):1113-21. [DOI:10.1177/193229681300700503] [PMID] [PMCID]
Bacarin TA, Sacco IC, Hennig EM. Plantar pressure distribution patterns during gait in diabetic neuropathy patients with a history of foot ulcers. Clinics. 2009; 64(2):113-20. [DOI:10.1590/S1807-59322009000200008] [PMID] [PMCID]
Dillon MP. Partial foot amputation: Aetiology, incidence, complications, prosthetic intervention and a characterisation of gait. New York: Center for International Rehabilitation Research Information and Exchange; 2010.
Waaijman R, de Haart M, Arts ML, Wever D, Verlouw AJ, Nollet F, et al. Risk factors for plantar foot ulcer recurrence in neuropathic diabetic patients. Diabetes Care. 2014; 37(6):1697-705. [DOI:10.2337/dc13-2470] [PMID]
Eliav E, Gracely RH. Measuring and assessing pain. Orofacial pain and headache. London: Elsevier Health Sciences; 2008. [DOI:10.1016/B978-0-7234-3412-2.10003-3]
Owings T, Apelqvist J, Stenström A, Becker M, Bus S, Kalpen A, et al. Plantar pressures in diabetic patients with foot ulcers which have remained healed. Diabetic Medicine. 2009; 26(11):1141-6. [DOI:10.1111/j.1464-5491.2009.02835.x] [PMID]
Frykberg RG, Lavery LA, Pham H, Harvey C, Harkless L, Veves A. Role of neuropathy and high foot pressures in diabetic foot ulceration. Diabetes Care. 1998; 21(10):1714-9. [DOI:10.2337/diacare.21.10.1714] [PMID]
Lavery LA, Armstrong DG, Wunderlich RP, Tredwell J, Boulton AJ. Predictive value of foot pressure assessment as part of a population-based diabetes disease management program. Diabetes Care. 2003; 26(4):1069-73. [DOI:10.2337/diacare.26.4.1069] [PMID]
Duckworth T, Boulton A, Betts R, Franks C, Ward J. Plantar pressure measurements and the prevention of ulceration in the diabetic foot. Journal of Bone & Joint Surgery, British Volume. 1985; 67(1):79-85. [DOI:10.1302/0301-620X.67B1.3968150]
Armstrong DG, Peters EJ, Athanasiou KA, Lavery LA. Is there a critical level of plantar foot pressure to identify patients at risk for neuropathic foot ulceration? The Journal of Foot and Ankle Surgery. 1998; 37(4):303-7. [DOI:10.1016/S1067-2516(98)80066-5]
Zarezadeh F, Arazpour M, Bahramizadeh M, Mardani MA, Head J. Design and construction of a new partial foot prosthesis based on high-pressure points in a patient with diabetes with transmetatarsal amputation: A technical note. Journal of Prosthetics and Orthotics. 2018; 30(2):108-13. [DOI:10.1097/JPO.0000000000000183]
Birke JA, Foto JG, Pfiefer LA. Effect of orthosis material hardness on walking pressure in high-risk diabetes patients. JPO: Journal of Prosthetics and Orthotics. 1999; 11(2):43-6. [DOI:10.1097/00008526-199901120-00007]
Tong JW, Ng EY. Preliminary investigation on the reduction of plantar loading pressure with different insole materials (SRP-Slow Recovery Poron, P-Poron, PPF-Poron+Plastazote, firm and PPS-Poron+Plastazote, soft). The Foot. 2010; 20(1):1-6. [DOI:10.1016/j.foot.2009.12.004] [PMID]
Owings TM, Woerner JL, Frampton JD, Cavanagh PR, Botek G. Custom therapeutic insoles based on both foot shape and plantar pressure measurement provide enhanced pressure relief. Diabetes Care. 2008; 31(5):839-44. [DOI:10.2337/dc07-2288] [PMID]
Nather A, Lin Wong K. Distal amputations for the diabetic foot. Diabetic Foot & Ankle. 2013; 4(1):21288. [DOI:10.3402/dfa.v4i0.21288] [PMID] [PMCID]
Dillon MP, Barker TM. Can partial foot prostheses effectively restore foot length? Prosthetics and Orthotics International. 2006; 30(1):17-23. [DOI:10.1080/03093640500467480] [PMID]
Ko M, Hughes L, Lewis H. Walking speed and peak plantar pressure distribution during barefoot walking in persons with diabetes. Physiotherapy Research International. 2012; 17(1):29-35. [DOI:10.1002/pri.509] [PMID]
Rezaeian Z, Karimi MT, Eshragh A. Evaluation of the efects of two types of foot rockers on the temporal-spatial gait parameters in diabetic patients. Archives of Rehabilitation. 2016; 17(2):168-77. [DOI:10.21859/jrehab-1702168]
Basu S, Yudkin JS, Kehlenbrink S, Davies JI, Wild SH, Lipska KJ, et al. Estimation of global insulin use for type 2 diabetes, 2018-30: A microsimulation analysis. The Lancet Diabetes & Endocrinology. 2019; 7(1):25-33. [DOI:10.1016/S2213-8587(18)30303-6]
Armstrong D, Lavery L. Clinical care of the diabetic foot. Arlington, Virginia: American Diabetes Association; 2010.
Apelqvist J. The Diabetic Foot Syndrome Today: A Pandemic Uprise. The Diabetic Foot Syndrome. 2018; 26(1):1-18. [DOI:10.1159/000480040]
Sage RA. Biomechanics of ambulation after partial foot amputation: prevention and management of reulceration. Journal of Prosthetics and Orthotics. 2007; 19(8):P77-P9. [DOI:10.1097/JPO.0b013e3180dc92fb]
Stills ML. Partial foot prostheses/orthoses. Clinical Prosthetics & Orthotics. 1987; 12(1):14-8.
Zhang M, Mak A. In vivo friction properties of human skin. Prosthetics and Orthotics International. 1999; 23(2):135-41.
Polyzois GL, Tarantili PA, Frangou MJ, Andreopoulos AG. Physical properties of a silicone prosthetic elastomer stored in simulated skin secretions. The Journal of Prosthetic Dentistry. 2000; 83(5):572-7. [DOI:10.1016/S0022-3913(00)70017-5]
Burger H, Erzar D, Maver T, Olenšek A, Cikajlo I, Matjačić Z. Biomechanics of walking with silicone prosthesis after midtarsal (Chopart) disarticulation. Clinical Biomechanics. 2009; 24(6):510-6. [DOI:10.1016/j.clinbiomech.2009.03.010] [PMID]
Pollard J, Hamilton GA, Rush SM, Ford LA. Mortality and morbidity after transmetatarsal amputation: retrospective review of 101 cases. The Journal of Foot and Ankle Surgery. 2006; 45(2):91-7. [DOI:10.1053/j.jfas.2005.12.011] [PMID]
Lange LR. The lange silicone partial foot prosthesis. Journal of Prosthetics and Orthotics. 1991; 4(1):56-61. [DOI:10.1097/00008526-199100410-00007]
Armstrong D, Lavery L. Plantar pressures are higher in diabetic patients following partial foot amputation. Ostomy/Wound Management. 1998; 44(3):30-2. [PMID]
Garbalosa JC, Cavanagh PR, Wu G, Ulbrecht JS, Becker MB, Alexander IJ, et al. Foot function in diabetic patients after partial amputation. Foot & Ankle International. 1996; 17(1):43-8. [DOI:10.1177/107110079601700110] [PMID]
Robinson CC, Balbinot LF, Silva MF, Achaval M, Zaro MA. Plantar pressure distribution patterns of individuals with prediabetes in comparison with healthy individuals and individuals with diabetes. Journal of Diabetes Science and Technology. 2013; 7(5):1113-21. [DOI:10.1177/193229681300700503] [PMID] [PMCID]
Bacarin TA, Sacco IC, Hennig EM. Plantar pressure distribution patterns during gait in diabetic neuropathy patients with a history of foot ulcers. Clinics. 2009; 64(2):113-20. [DOI:10.1590/S1807-59322009000200008] [PMID] [PMCID]
Dillon MP. Partial foot amputation: Aetiology, incidence, complications, prosthetic intervention and a characterisation of gait. New York: Center for International Rehabilitation Research Information and Exchange; 2010.
Waaijman R, de Haart M, Arts ML, Wever D, Verlouw AJ, Nollet F, et al. Risk factors for plantar foot ulcer recurrence in neuropathic diabetic patients. Diabetes Care. 2014; 37(6):1697-705. [DOI:10.2337/dc13-2470] [PMID]
Eliav E, Gracely RH. Measuring and assessing pain. Orofacial pain and headache. London: Elsevier Health Sciences; 2008. [DOI:10.1016/B978-0-7234-3412-2.10003-3]
Owings T, Apelqvist J, Stenström A, Becker M, Bus S, Kalpen A, et al. Plantar pressures in diabetic patients with foot ulcers which have remained healed. Diabetic Medicine. 2009; 26(11):1141-6. [DOI:10.1111/j.1464-5491.2009.02835.x] [PMID]
Frykberg RG, Lavery LA, Pham H, Harvey C, Harkless L, Veves A. Role of neuropathy and high foot pressures in diabetic foot ulceration. Diabetes Care. 1998; 21(10):1714-9. [DOI:10.2337/diacare.21.10.1714] [PMID]
Lavery LA, Armstrong DG, Wunderlich RP, Tredwell J, Boulton AJ. Predictive value of foot pressure assessment as part of a population-based diabetes disease management program. Diabetes Care. 2003; 26(4):1069-73. [DOI:10.2337/diacare.26.4.1069] [PMID]
Duckworth T, Boulton A, Betts R, Franks C, Ward J. Plantar pressure measurements and the prevention of ulceration in the diabetic foot. Journal of Bone & Joint Surgery, British Volume. 1985; 67(1):79-85. [DOI:10.1302/0301-620X.67B1.3968150]
Armstrong DG, Peters EJ, Athanasiou KA, Lavery LA. Is there a critical level of plantar foot pressure to identify patients at risk for neuropathic foot ulceration? The Journal of Foot and Ankle Surgery. 1998; 37(4):303-7. [DOI:10.1016/S1067-2516(98)80066-5]
Zarezadeh F, Arazpour M, Bahramizadeh M, Mardani MA, Head J. Design and construction of a new partial foot prosthesis based on high-pressure points in a patient with diabetes with transmetatarsal amputation: A technical note. Journal of Prosthetics and Orthotics. 2018; 30(2):108-13. [DOI:10.1097/JPO.0000000000000183]
Birke JA, Foto JG, Pfiefer LA. Effect of orthosis material hardness on walking pressure in high-risk diabetes patients. JPO: Journal of Prosthetics and Orthotics. 1999; 11(2):43-6. [DOI:10.1097/00008526-199901120-00007]
Tong JW, Ng EY. Preliminary investigation on the reduction of plantar loading pressure with different insole materials (SRP-Slow Recovery Poron, P-Poron, PPF-Poron+Plastazote, firm and PPS-Poron+Plastazote, soft). The Foot. 2010; 20(1):1-6. [DOI:10.1016/j.foot.2009.12.004] [PMID]
Owings TM, Woerner JL, Frampton JD, Cavanagh PR, Botek G. Custom therapeutic insoles based on both foot shape and plantar pressure measurement provide enhanced pressure relief. Diabetes Care. 2008; 31(5):839-44. [DOI:10.2337/dc07-2288] [PMID]
Nather A, Lin Wong K. Distal amputations for the diabetic foot. Diabetic Foot & Ankle. 2013; 4(1):21288. [DOI:10.3402/dfa.v4i0.21288] [PMID] [PMCID]
Dillon MP, Barker TM. Can partial foot prostheses effectively restore foot length? Prosthetics and Orthotics International. 2006; 30(1):17-23. [DOI:10.1080/03093640500467480] [PMID]
Ko M, Hughes L, Lewis H. Walking speed and peak plantar pressure distribution during barefoot walking in persons with diabetes. Physiotherapy Research International. 2012; 17(1):29-35. [DOI:10.1002/pri.509] [PMID]
Rezaeian Z, Karimi MT, Eshragh A. Evaluation of the efects of two types of foot rockers on the temporal-spatial gait parameters in diabetic patients. Archives of Rehabilitation. 2016; 17(2):168-77. [DOI:10.21859/jrehab-1702168]
نوع مطالعه: پژوهشی |
موضوع مقاله:
اورتز و پروتز
دریافت: 1397/10/24 | پذیرش: 1398/3/7 | انتشار: 1398/4/10
دریافت: 1397/10/24 | پذیرش: 1398/3/7 | انتشار: 1398/4/10
ارسال پیام به نویسنده مسئول
| بازنشر اطلاعات | |
 |
این مقاله تحت شرایط Creative Commons Attribution-NonCommercial 4.0 International License قابل بازنشر است. |